Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
\(n_{HCl}=4.100:1000=0,4\left(mol\right)\)
a. PTHH: MgO + 2HCl ---> MgCl2 + H2O
Ta thấy: \(\dfrac{0,1}{1}< \dfrac{0,4}{2}\)
Vậy HCl dư.
=> \(n_{dư}=\dfrac{0,1.2}{0,4}=0,5\left(mol\right)\)
=> \(m_{dư}=0,5.36,5=18,2\left(g\right)\)
b. Ta có: \(V_{dd_{MgCl_2}}=V_{HCl}=\dfrac{100}{1000}=0,1\left(lít\right)\)
Theo PT: \(n_{MgCl_2}=n_{MgO}=0,1\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,1}{0,1}=1M\)

nCuO=2,4/80=0,03(mol)
m(H2SO4)=29,4%.100=29,4(g) -> nH2SO4=29,4/98=0,3(mol)
a) PTHH: CuO + H2SO4 -> CuSO4 + H2O
Ta có: 0,03/1 < 0,3/1
b)=> CuO hết, H2SO4 dư => Tính theo nCuO
nH2SO4(p.ứ)=nCuSO4=nCuO=0,03(mol)
=>nH2SO4(dư)=0,3-0,03=0,27(mol)
=>mH2SO4(dư)=0,27. 98= 26,46(g)
b) mCuSO4=0,03.160= 4,8(g)
mddsau= 2,4+ 100=102,4(g)
C%ddCuSO4= (4,8/102,4).100=4,6875%
C%ddH2SO4(dư)= (26,46/102,4).100= 25,84%
Số mol của đồng (II) oxit
nCuO = \(\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{2,4}{80}=0,03\left(mol\right)\)
Khối lượng của axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{29,4.100}{100}=29,4\left(g\right)\)
Số mol của axit sunfuric
nH2SO4 = \(\dfrac{m_{H2SO4}}{M_{H2SO4}}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
a) Pt : CuO + H2SO4 → CuSO4 + H2O\(|\)
1 1 1 1
0,03 0,3 0,03
b) Lập tỉ số so sánh : \(\dfrac{0,03}{1}< \dfrac{0,3}{1}\)
⇒ CuO phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của CuO
Số mol dư của axit sunfuric
ndư = nban đầu - nmol
= 0,3 - (0,03 . 1)
= 0,27 (mol)
Khối lượng dư của axit sunfuric
mdư = ndư . MH2SO4
= 0,27 . 98
= 26,46 (g)
c) Số mol của đồng (II) sunfat
nCuSO4 = \(\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
Khối lượng của đồng (II) sunfat
mCuSO4 = nCuSO4 . MCuSO4
= 0,03 . 160
= 4,8 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mCuO + mH2SO4
= 2,4 + 100
= 102,4 (g)
Nồng độ phần trăm của đồng (II) sunfat
C0/0CuSO4= \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{4,8.100}{102,4}=4,6875\)0/0
Nồng độ phần trăm của axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{26,46.100}{102,4}=25,84\)0/0
Chúc bạn học tốt

a)
$n_{Fe} = \dfrac{11,2}{56} = 0,2(mol) ; n_{HCl} = 0,1.2 = 0,2(mol)$
$Fe + 2HCl \to FeCl_2 + H_2$
Ta thấy :
$n_{Fe} : 1 > n_{HCl} : 2$ nên Fe dư
$n_{H_2} = \dfrac{1}{2}n_{HCl} = 0,1(mol)$
$V_{H_2} = 0,1.22,4 = 2,24(lít)$
b)
$n_{Fe\ pư} = n_{H_2} = 0,1(mol)$
$\Rightarrow m_{Fe\ dư} = 11,2 - 0,1.56 = 5,6(gam)$
c)
$n_{FeCl_2} = n_{Fe\ pư} = 0,1(mol)$
$C_{M_{FeCl_2}} = \dfrac{0,1}{0,1} = 1M$

\(n_{BaCl_2}=\dfrac{4,16}{208}=0,02 \left(mol\right)\)
\(n_{AgNO_3}=\dfrac{3,4}{170}=0,02\left(mol\right)\)
\(BaCl_2+2AgNO_3\rightarrow2AgCl+Ba\left(NO_3\right)_2\)
0,01 <----- 0,02 --------------------> 0,01
Do \(\dfrac{0,02}{1}>\dfrac{0,02}{2}\) => \(BaCl_2\) dư và dư: \(0,02-0,01=0,01\left(mol\right)\)
b.
Dung dịch sau phản ứng gồm \(BaCl_2\) dư và \(Ba\left(NO_3\right)_2\)
c.
\(CM_{Ba\left(NO_3\right)_2}=\dfrac{0,01}{0,2}=0,05M\)
\(CM_{BaCl_2}=\dfrac{0,01}{0,2}=0,05M\)

– Số mol KMnO4 = 0,2 (mol); số mol KOH = 2 (mol)
– Phương trình phản ứng:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,2 0,5
* Ở điều kiện nhiệt độ thường:
Cl2 + 2KOH → KCl + KClO + H2O
0,5 1,0 0,5 0,5
– Dư 1,0 mol KOH
CM (KCl) = CM (KClO) = 0,5 (M); CM (KOH dư) = 1 (M)
* Ở điều kiện đun nóng trên 700C:
3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
0,5 1,0 5/6 1/6
– Dư 1,0 mol KOH
CM (KCl) = 5/6 (M); CM (KClO3) = 1/6 (M); CM (KOH dư) = 1 (M).

a) \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right);n_{H_2SO_4}=0,3.1=0,03\left(mol\right)\)
PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
b) Xét tỉ lệ: \(\dfrac{0,1}{2}>\dfrac{0,03}{3}\) => Al dư, H2SO4 hết, tính theo H2SO4
Theo PTHH: \(n_{Al\left(p\text{ư}\right)}=\dfrac{2}{3}.n_{H_2SO_4}=\dfrac{2}{3}.0,03=0,02\left(mol\right)\)
`=>` \(n_{Al\left(d\text{ư}\right)}=0,1-0,02=0,08\left(mol\right)\)
c) Theo PTHH: \(n_{H_2}=n_{H_2SO_4}=0,03\left(mol\right)\)
`=>` \(V_{H_2}=0,03.22,4=0,672\left(l\right)\)

\(n_{Al_2O_3}=\dfrac{30,6}{102}=0,3(mol)\\ n_{HCl}=\dfrac{100.21,9}{100.36,5}=0,6(mol)\\ a,PTHH:Al_2O_3+6HCl\to 2AlCl_3+3H_2O\)
\(b,\)Vì \(\dfrac{n_{Al_2O_3}}{1}>\dfrac{n_{HCl}}{6}\) nên \(Al_2O_3\) dư
\(n_{Al_2O_3(dư)}=0,3-\dfrac{1}{6}.0,6=0,2(mol)\\ \Rightarrow m_{Al_2O_3(dư)}=0,2.102=20,4(g)\\ c,n_{AlCl_3}=\dfrac{1}{3}.0,6=0,2(mol)\\ \Rightarrow C\%_{AlCl_3}=\dfrac{0,2.133,5}{100+30,6}.100\%=20,44\%\\ C\%_{Al_2O_3(dư)}=\dfrac{20,4}{100+30,6}.100\%=15,62\%\)

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
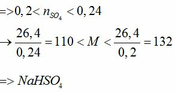
b)
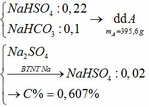
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O



Câu 3 :
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
100ml = 0,1l
\(n_{HCl}=2,5.0,1=0,25\left(mol\right)\)
a) Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,1 0,25 0,1
b) Lập tỉ số so sánh : \(\dfrac{0,1}{1}< \dfrac{0,25}{2}\)
⇒ Mg phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của Mg
\(n_{HCl\left(dư\right)}=0,25-\left(0,1.2\right)=0,05\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,05.36,5=1,825\left(g\right)\)
c) \(n_{MgCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(C_{M_{MgCl2}}=\dfrac{0,1}{0,1}=1\left(M\right)\)
\(C_{M_{HCl\left(dư\right)}}=\dfrac{0,05}{0,1}=0,5\left(M\right)\)
Chúc bạn học tốt