Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3. Khối lượng mol của hợp chất đó là :
2.28 = 56 (g/mol)
mC = \(\frac{56.85,7}{100}\approx48\left(g\right)\)
mH = 56 - 48 = 8 (g)
nC = \(\frac{48}{12}=4\left(mol\right)\)
nH = \(\frac{8}{1}=8\left(mol\right)\)
Vậy công thức hóa học là C4H8.

1/Đặt Z, N lần lượt là số hạt p, n có trong nguyên tử M
ta có hệ phương trình
\(\begin{cases}2Z+N=79+3\\2Z-N=19+3\end{cases}\)\(\Rightarrow\begin{cases}Z=26\\N=30\end{cases}\)
a. Cấu hình electron nguyên tử của M là: 1s22s22p63s23p63d64s2
M ở ô thứ 26, chu kì 4 nhóm VIIIB trong bảng tuần hoàn.
b. Cấu hình electron của ion Fe2+ là: 1s22s22p63s23p63d6
Cấu hình electron của ion Fe3+ là: 1s22s22p63s23p63d5
2.
Vì R tạo được hợp chất khí với H nên R là phi kim.
Giả sử R thuộc nhóm x (x\(\ge\)4).
Theo giả thiết
công thức của R với H là RH8-x \(\Rightarrow\)a=\(\frac{R}{R+8-x}.100\)
công thức oxit cao nhất của R là R2Ox
\(\Rightarrow\) b=\(\frac{2R}{2R+16x}.100\) \(\Leftrightarrow\) b= \(\frac{R}{R+8x}.100\)
suy ra \(\frac{a}{b}=\frac{R+8x}{R+8-x}=\frac{11}{4}\)\(\Leftrightarrow R=\frac{43x-88}{7}\)
Xét bảng
a/ Vậy R là C
b/
Công thức của R với H là CH4
Công thức electron ; Công thức cấu tạo
Oxti cao nhất của R là CO2
Công thức electron O:: C ::O; Công thức cấu tạo O=C=O
c.
Trong hợp chất CH4 có \(\Delta\chi=\chi_C-\chi_H\)=2,55-0,22=0,35<0,4 nên liên kết giữa C-H là liên kết cộng hóa trị không cực
Trong hợp chất CO2 có 0, \(\Delta\chi=\chi_O-\chi_C\) =3,44-2,55=0,89
\(\Rightarrow\) 0,4<\(\Delta\chi=0,89\)<1,7 nên liên kết giữa C=O là liên kết cộng hóa trị phân cực

Chọn C
- Xác định X:
Theo bài ra ta có hệ phương trình:
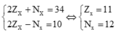
Cấu hình electron của X là: [Ne]3s1 → X là kim loại nhóm IA
X có xu hướng nhường 1e khi hình thành liên kết hóa học:
X → X+ + 1e
- Cấu hình electron của Y là: [He]2s22p5 → Y là phi kim nhóm VIIA hoặc từ kí hiệu nguyên tử xác định Y là Flo.
Y có xu hướng nhận 1e khi hình thành liên kết hóa học:
Y + 1e → Y-
Vậy hợp chất tạo thành là XY; liên kết trong hợp chất là liên kết ion.

Đáp án A.
+ Nguyên tố thuộc nhóm I, II, III không có số oxi hóa âm.
+ nO + | nH | = 8
Đề cho | nO | = | nH | => A thuộc nhóm IV
Đề cho | mO | = 3| mH | => mO = 3| 8 - mO | => mO = 6 => Y thuộc nhóm VI
Y thuộc nhóm VI có : O(16) , S(32) , Se (79)
=> X tương ứng là: C(12) , Si(14)
Biết X có số oxi hóa cao nhất trong M
=> Xcó số oxi hóa = nO = +4
=> M có dạng : XY2

Cấu hình electron của nguyên tử Mg: 1s22s22p63s2.
Mg có 2e ở lớp ngoài cùng nên thể hiện tính kim loại, hóa trị cao nhất với oxi là II, chất MgO là oxit bazơ và Mg(OH)2 là bazơ.

Br thuộc nhóm VIIA, chu kì 4 có 35 electron nên cấu hình theo lớp electron là 2, 8, 18, 7. Nó có 7e lớp ngoài cùng nên là phi kim. Hóa trị cao nhất với oxi là VII. Hóa trị trong hợp chất khí với hiđro là I và có công thức phân tử là HBr.



a: \(\left\{{}\begin{matrix}2Z+N=48\\2Z=2N\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z=16\\N=16\end{matrix}\right.\)
Số hiệu nguyên tử là 16
Số khối là 32
X là lưu huỳnh(S)
b: X là phi kim
Hóa trị cao nhất trong hợp chất với Oxi là 3
Hóa trị trong hợp chất với Hidro là 2