Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

mCO2 = 13.4 - 6.8 = 6.6 > nCO2 = 0.15mol.
nNaOH = 0.075 mol > nCO2 = 2nNaOH > muối NaHCO3 với m = 6.3g

Đáp án D
nH2SO4 = 0,565 mol ; nSO2 = 0,015 mol
+) Phần 1 : Mkhí = 32,8g ; nkhí = 0,0625 mol
Hỗn hợp khí không màu có 1 khí hóa nâu là NO và N2O
=> nNO = 0,05 ; nN2O = 0,0125 mol
Muối thu được là muối sunfat => có S trog D
Qui hỗn hợp D về dạng : Al (x mol) ; O (y mol) ; S (z mol)
Giả sử phản ứng D + HNO3 tạo t mol NH4+
Bảo toàn e : 3nAl + 6nS = 2nO + 3nNO + 8nN2O + 8nNH4
=>3x + 6z = 2y + 0,15 + 0,1 + 8t(1)
Muối sunfat thu được có : NH4+ ; Al3+ ; SO42-
Bảo toàn điện tích : nNH4 + 3nAl = 2nSO4
=>t + 3x = 2z(2)
Khi Cho dung dịch muối này phản ứng với NaOH vừa đủ thì :
Al3+ + 4OH- -> AlO2- + 2H2O
NH4+ + OH- -> NH3 + H2O
=> nNaOH = 4x + t = 0,13(3)
+) Phần 2 : (Al ; O ; S) + O2(không khí) -> ( 0,5x mol Al2O3) + SO2 ↑
=> mgiảm = mS – mO thêm
=>1,36 = 32z – 16.(1,5x – y)(4)
Giải hệ (1,2,3,4) => x = y = 0,03 ; z = 0,05 ; t = 0,01 mol
Vậy D có : 0,02 mol Al2O3 ; 0,02 mol Al ; 0,1 mol S
Bảo toàn e : 2nSO2 + 6nS = 3nAl pứ => nAl pứ = 0,21 mol
nH2SO4 = 3nAl2O3 pứ + (1,5nAl + nSO2 + nS)
=> nAl2O3 = 0,045 mol
Vậy hỗn hợp đầu có : 0,065 mol Al2O3 và 0,23 mol Al
=> m = 12,84g

Giải thích:
nH2SO4 = 0,565 mol ; nSO2 = 0,015 mol
+) Phần 1 : Mkhí = 32,8g ; nkhí = 0,0625 mol
Hỗn hợp khí không màu có 1 khí hóa nâu là NO và N2O
=> nNO = 0,05 ; nN2O = 0,0125 mol
Muối thu được là muối sunfat => có S trog D
Qui hỗn hợp D về dạng : Al (x mol) ; O (y mol) ; S (z mol)
Giả sử phản ứng D + HNO3 tạo t mol NH4+
Bảo toàn e : 3nAl + 6nS = 2nO + 3nNO + 8nN2O + 8nNH4
=> 3x + 6z = 2y + 0,15 + 0,1 + 8t (1)
Muối sunfat thu được có : NH4+ ; Al3+ ; SO42-
Bảo toàn điện tích : nNH4 + 3nAl = 2nSO4
=> t + 3x = 2z (2)
Khi Cho dung dịch muối này phản ứng với NaOH vừa đủ thì :
Al3+ + 4OH- -> AlO2- + 2H2O
NH4+ + OH- -> NH3 + H2O
=> nNaOH = 4x + t = 0,13 (3)
+) Phần 2 : (Al ; O ; S) + O2(không khí) -> ( 0,5x mol Al2O3) + SO2 ↑
=> mgiảm = mS – mO thêm
=> 1,36 = 32z – 16.(1,5x – y) (4)
Giải hệ (1,2,3,4) => x = y = 0,03 ; z = 0,05 ; t = 0,01 mol
Vậy D có : 0,02 mol Al2O3 ; 0,02 mol Al ; 0,1 mol S
Bảo toàn e : 2nSO2 + 6nS = 3nAl pứ => nAl pứ = 0,21 mol
nH2SO4 = 3nAl2O3 pứ + (1,5nAl + nSO2 + nS)
=> nAl2O3 = 0,045 mol
Vậy hỗn hợp đầu có : 0,065 mol Al2O3 và 0,23 mol Al
=> m = 12,84g
Đáp án D

Đáp án B
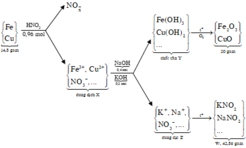
n H N O 3 = 0,96 mol và n N a O H = 0,4 mol, n K O H = 0,2
đặt n F e = x mol và n C u = y mol
Bảo toàn nguyên tố có n F e 2 O 3 = ½ . n F e = ½ .x
n C u O = n C u = y
Ta có hệ phương trình sau 56x + 64 y = 14,8 gam và 80x + 80y = 20
→ x = 0,15 mol và y = 0,1 mol
Nếu dung dịch Z chỉ chứa 2 muối N a N O 3 và K N O 3 thì khi đun nóng thu được K N O 2 và N a N O 2
Bảo toàn nguyên tố có n N a N O 2 = n N a O H = 0,4 và n K O H = 0,2 = n K N O 2
→ mrắn = 0,4.69 +0,2. 85 = 44,6 gam > 42,86 nên Z còn chứa cả NaOH và KOH
Z chứa : N a + : 0,4 mol; K + : 0,2 mol; OH- : a mol và N O 3 - : b mol
Bảo toàn điện tích có 0,4 + 0,2 = a + b (*)
Đun nóng Z có 0,4 mol Na ; K + : 0 , 2 m o l ; O H - : a m o l v à N O 2 - : b m o l
→ 17a + 46b + 0,2.39 + 0,4.23 = 42,86 (**)
Từ (*) và (**) → a = 0,06 và b = 0,54
→ dd X chứa F e 2 + : c m o l ; F e 3 + : d m o l v à C u 2 + : 0 , 1 m o l ; N O 3 - : 0 , 54 m o l (cùng bằng lượng NO3- trong Z)
Bảo toàn điện tích có 2c + 3d + 0,1.2 = 0,54 (***)
Bảo toàn Fe có c + d =0,15 (****)
Từ (***) và (****) → c = 0,11 và d =0,04 mol
Bảo toàn nguyên tố có n N (sp khử) = n H N O 3 – n N O 3 (Y) = 0,96 – 0,54 =0,42 mol
Quy đổi khí sản phẩm khử là N : 0,42 mol và O : e mol
Bảo toàn e có 2 n F e ( 2 + ) + 3 n F e ( 3 + ) + 2 n C u ( 2 + ) - 2 n O = 5 n N
→ 5.0,42 = 2.0,11 +3.0,04 + 0,1.2 +2e
→ e = 0,78 mol
Bảo toàn khối lượng mdd X = m K L + m H N O 3 – m N – m O
= 14,8 + 126 – 0,42.14 – 0,78.16 =122,44 g
Nồng độ % của F e N O 3 3 là := 7,9%

mMOH = 7,2 gam => nMOH = 7,2/(M+17) g/mol
Khối lượng nước m = 36 - 7,2 = 28,8 gam
=> nH2O = 1,6 mol
nH2 = 0,57 mol
BTKL: m este = mX + mY – mdd MOH = 33,4 + 12,8 – 36 => m = 10,2 gam
E là este no, đơn chức, mạch hở nên X là ancol no, đơn chức, mạch hở ROH
X gồm H2O (1,6 mol) và ROH trong đó mROH = mX – mH2O = 33,4 – 28,8 = 4,6 gam
2H2O + 2Na → 2NaOH + H2
1,6 → 0,8 mol
ROH + Na → RONa + 0,5H2
0,1 ← 0,05 mol
=> MROH = 46. vậy ROH là C2H5OH
Ta có mol este = số mol ancol => neste = 0,1=> M este = 102 (C5H10O2) => E là C2H5COOC2H5
Y gồm C2H5COOM (0,1 mol) và MOH dư (a mol)
BTNT M: nMOH ban đầu = 2.nM2CO3
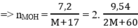
=> M là Na
=> mC2H5COONa = 9,6 gam => mNaOH dư = 12,8 – 9,6 = 3,2 gam => nNaOH dư = 0,08 m
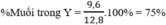
Đáp án cần chọn là: A

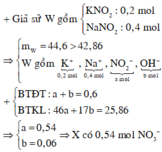
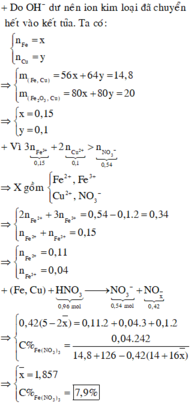

Đáp án : D
Gọi CT chung của 2 muối cacbonat kim loại hóa trị II là RCO3
RCO3 → (đk :t0) RO + CO2
Áp dụng định luật bảo toàn khối lượng ta có :
m CO2 = m RCO3 - mRO = 13,4 – 6,8 = 6,6 g
=> n CO2 = 0,15 mol
Ta có :
n NaOH = 0,075 mol
=> k = n NaOH / nCO2 = 0,075 / 0,15 = 0,5 < 1
=> Tạo muối NaHCO3 và CO2 dư
CO2 + NaOH → NaHCO3
0,075 0,075
=> mmuối = 0,075. 84 = 6,3 g