Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi \(\left\{{}\begin{matrix}n_{N_2}=x\left(mol\right)\\n_{H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\dfrac{28x+2y}{x+y}=12,4\)
\(\Leftrightarrow12,4x+12,4y-28x-2y=0\Leftrightarrow-15,6x=-10,4y\\ \Leftrightarrow\dfrac{x}{y}=-\dfrac{10,4}{-15,6}=\dfrac{2}{3}\)
Giả sử \(\left\{{}\begin{matrix}n_{N_2}=2\left(mol\right)\\n_{H_2}=3\left(mol\right)\end{matrix}\right.\)
\(n_{khí.giảm}=n_{NH_3}=\dfrac{2}{3}n_{H_2}.H\%=\dfrac{2}{3}.3.40\%=0,8\left(mol\right)\)
\(n_Y=2+3-0,8=4,2\left(mol\right)\)
\(m_Y=m_X=28.2+2.3=62\left(g\right)\)
\(\overline{M_Y}=\dfrac{62}{4,2}=14,76g/mol\)
\(n_{N_2}=a;n_{H_2}=b\\ PT:\dfrac{1}{2}N_2+\dfrac{3}{2}H_2-Fe,t^{^0}->NH_3\\ M_X=\dfrac{28a+2b}{a+b}=12,4\\ a=1,5b\\ Sau.pư:\\ M_Y=\dfrac{2.0,6b+28\left(a-\dfrac{0,4b}{3}\right)+17.0,4b}{0,6b+a-\dfrac{0,4b}{3}+0,4b}=19,55\)

Đáp án C
Đặt số mol hỗn hợp khí X là 1 mol.
Gọi số mol NH3 là x mol suy ra số mol NH3 phân hủy là 0,15.x (mol)
Khối lượng phân tử trung bình của X:
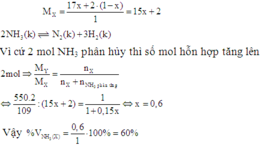

Đáp án B
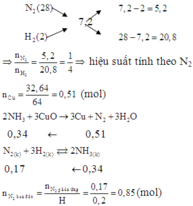
Hỗn hợp ban đầu chứa N 2 : 0 , 2 H 2 : 0 , 8
→ Hiệu suất tính theo N2.
nsau = 3,6/4 = 0,9 → N2 phản ứng = 0,05 → H = 25%

Xét `a<b->H` tính theo `Fe.`
`Fe+S` $\xrightarrow{t^o}$ `FeS`
`0,5a->0,5a->0,5a(mol)`
Có `n_{Fe\ pu}=0,5a(mol)`
`Y` gồm `Fe:0,5a(mol);S:b-0,5a(mol);FeS:0,5a(mol)`
`FeS+2HCl->FeCl_2+H_2S`
`Fe+2HCl->FeCl_2+H_2`
Theo PT: `n_{H_2S}=n_{FeS}=0,5a(mol);n_{H_2}=n_{Fe}=0,5a(mol)`
`->{n_{H_2S}}/{n_{H_2}}={5.2-2}/{34-5.2}=1/3`
``->{0,5a}/{0,5a}=1/3` vô lí.
Xét `a>b->H` tính theo `S.`
`Fe+S` $\xrightarrow{t^o}$ `FeS`
`0,5b←0,5b->0,5b(mol)`
Có `n_{S\ pu}=0,5b(mol)`
`Y` gồm `Fe:a-0,5b(mol);S:0,5b(mol);FeS:0,5b(mol)`
`FeS+2HCl->FeCl_2+H_2S`
`Fe+2HCl->FeCl_2+H_2`
Theo PT: `n_{H_2S}=n_{FeS}=0,5b(mol);n_{H_2}=n_{Fe}=a-0,5b(mol)`
`->{n_{H_2S}}/{n_{H_2}}={5.2-2}/{34-5.2}=1/3`
``->{0,5b}/{a-0,5b}=1/3`
`->1,5b=a-0,5b`
`->a=2b`
`->a:b=2:1`

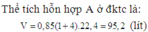

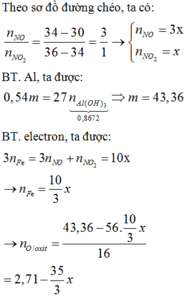

\(n_{N_2}=a,n_{H_2}=b\\ M_A=\dfrac{28a+2b}{a+b}=7,2\\ a=4b\\ PT:\dfrac{1}{2}N_2+\dfrac{3}{2}H_2-Fe,t^{^0}->NH_3\\ CuO+H_2-t^{^0}->Cu+H_2O\\ n_{Cu}=n_{H_2dư}=\dfrac{32,64}{64}=0,51mol\\ n_{H_2pư}=b-0,51\left(mol\right)\\ H=\dfrac{b-0,51}{b}=0,2\\ b=0,6375\\ a=2,55\\ V_A=22,4\left(0,6375+2,55\right)=71,4L\)