Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH :
Fe + H2SO4 -> FeSO4 + H2
x.......................................x (mol)
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
y.................................................1,5y (mol)
2Fe + 6H2SO4(đ,n) -> Fe2(SO4)3 + 6H2O + 3SO2
x .....................................................................1,5x (mol)
2Al + 6H2SO4(đ,n) -> Al2(SO4)3 + 6H2O + 3SO2
y........................................................................1,5y (mol)
Cu + 2H2SO4(đ,n) -> CuSO4 + 2H2O + SO2
z................................................................z (mol)
Gọi x,y,z lần lượt là số mol Fe , Al , Cu trong hỗn hợp
khi đó 56x + 27y + 64z = 17,4(g) (1)
\(\Sigma n_{H2}=x+1,5y=\dfrac{8,96}{22,4}=0,4\left(mol\right)\) (2)
\(\Sigma n_{SO2}=1,5x+1,5y+z=\dfrac{12,32}{22,4}=0,55\left(mol\right)\) (3)
Từ (1) , (2) và (3 ) ta có hệ :
\(\left\{{}\begin{matrix}56x+27y+64z=17,4\\x+1,5y=0,4\\1,5x+1,5y+z=0,55\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,2\left(mol\right)\\z=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=5,6\left(g\right)\\m_{Al}=5,4\left(g\right)\\m_{Cu}=6,4\left(g\right)\end{matrix}\right.\)
==================================
* chú ý : cái chỗ mình viết PTHH (đ,n ) là đặc nóng nhé :) -- không phải đặc nguội
hoặc có thể viết H2SO4 đặc nóng ntn để phân biệt giữa đặc nóng và đặc nguội
\(Cu+2H2SO4_{\left(\text{đ}\right)}-^{t0}->C\text{uS}O4+SO2\uparrow+2H2O\)
viết thế này thì ngta cx có thể hiểu H2SO4 đặc nóng (:

Gọi x,y lần lượt là số mol Mg, Fe
Mg + S ⟶ MgS
Fe + S ⟶ FeS
MgS + 4H2SO4 → MgSO4 + 4H2O + 4SO2
2FeS + 10H2SO4 → Fe2(SO4)3 + 9SO2 + 10H2O
S + 2H2SO4 → 3SO2 + 2H2O
Ta có :
\(\left\{{}\begin{matrix}Mg:x\left(mol\right)\\Fe:y\left(mol\right)\end{matrix}\right.\underrightarrow{+S:0,5\left(mol\right)}\left\{{}\begin{matrix}MgS:x\left(mol\right)\\FeS:y\left(mol\right)\\S_{dư}:0,5-\left(x+y\right)\left(mol\right)\end{matrix}\right.\underrightarrow{+H_2SO_4}\left\{{}\begin{matrix}MgSO_4:x\left(mol\right)\\Fe_2\left(SO_4\right)_3:\dfrac{y}{2}\left(mol\right)\\SO_2\end{matrix}\right.\underrightarrow{+NaOH\left(dư\right)}\left(kt\right)\left\{{}\begin{matrix}Mg\left(OH\right)_2:x\left(mol\right)\\Fe\left(OH\right)_3:y\left(mol\right)\end{matrix}\right.\underrightarrow{to}\left\{{}\begin{matrix}MgO:x\left(mol\right)\\Fe_2O_3:\dfrac{y}{2}\left(mol\right)\end{matrix}\right.\)
Ta có :\(n_{SO_2}=4x+4,5y+\left[0,5-\left(x+y\right)\right].3=2\left(mol\right)\)
\(40x+160\dfrac{y}{2}=24\)
=> \(\left\{{}\begin{matrix}x=0,2\\y=0,2\end{matrix}\right.\)
=> \(m_{Mg}=0,2.24=4,8\left(g\right)\)
\(m_{Fe}=0,2.56=11,2\left(g\right)\)
\(m=4,8+11,2=16\left(g\right)\)
\(\%m_{Mg}=\dfrac{4,8}{16}.100=30\%\)
\(\%m_{Fe}=100-30=70\%\)

Bài giải:
2Fe + 6H2SO4 -> Fe2(SO4)3 + 3SO2 + 6H2O
2Al + 6H2SO4 -> Al2(SO4)3 + 3SO2 + 6H2O
Cu + 2H2SO4 -> CuSO4 + SO2 + 2H2O
(chú ý là H2SO4 đặc, nóng sẽ khử kim loại tạo muối sunfat kim loại có hóa trị cao nhất)
Lượng 3 muối sunfat = 45,1.2 = 90,2 gam và số mol SO2 = 0,7 mol
Fe2(SO4)3 + 6NaOH -> 2Fe(OH)3 + 3Na2SO4
Al2(SO4)3 + 6NaOH -> 2Al(OH)3 + 3Na2SO4
CuSO4 + 2NaOH -> Cu(OH)2 + Na2SO4
Al(OH)3 + NaOH -> NaAlO2 + H2O
Kết tủa lọc được chỉ còn Fe(OH)3 và Cu(OH)2
2Fe(OH)3 -> Fe2O3 + 3H2O
Cu(OH)2 -> CuO + H2O
12.2 = 24 (gam) là tổng lượng 2 oxit Fe2O3 + CuO
Gọi x, y, z lần lượt là số mol của Fe, Al, Cu
Ta có hệ 3 phương trình:
1,5x + 1,5y + z = 0,7
200x + 171y + 160z = 90,2
80x + 80z = 24
Giải hệ cho x = 0,2 ; y = 0,2 ; z = 0,1
Suy ra khối lượng mỗi kim loại trong hỗn hợp ban đầu: mFe = 11,2 g ; mAl = 5,4 g ; mCu = 6,4 g
\\ok//

\(n_{SO_2}=\dfrac{13,644}{22,4}=0,61\left(mol\right)\)
Đặt n Fe = x (mol) =>\(m_{Fe}=56x\)
Vì m Fe = mMg => \(n_{Mg}=\dfrac{56x}{24}=\dfrac{7}{3}x\)
nAl = y(mol)
=> 56x + 56x + 27y = 16,14 (1)
\(Fe\rightarrow Fe^{3+}+3e\) \(S^{+6}+2e\rightarrow S^{+4}\)
\(Mg\rightarrow Mg^{2+}+2e\)
\(Al\rightarrow Al^{3+}+3e\)
Bảo toàn e : 3x + \(\dfrac{7}{3}.2x\) + 3y = 0,61.2 (2)
Từ (1), (2) => x=0,12 ; y=0,1
=> mFe =mMg=0,12.56 = 6,72(g)
m Al = 0,1.27=2,7(g)

Gọi $n_{Fe} = a ; n_{Mg} = b; n_{Al} = c$
Ta có :
$24b = 56a(1)$
$56a + 24b + 27c = 16,14(2)$
$n_{SO_2} = 0,61(mol)$
Bảo toàn electron : $3n_{Fe} + 2n_{Mg} + 3n_{Al} = 2n_{SO_2}$
$\Rightarrow 3a + 2b + 3c = 0,61.2(3)$
Từ (1)(2)(3) suy ra a = 0,12 ; b = 0,28 ; c = 0,1
$m_{Fe} = m_{Mg} = 0,12.56 = 6,72(gam)$
$m_{Al} = 0,1.27 = 2,7(gam)$

a, Ta có: 27nAl + 56nFe = 27,8 (1)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{17,353}{24,79}=0,7\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{27,8}.100\%\approx19,42\%\\\%m_{Fe}\approx80,58\%\end{matrix}\right.\)
b, \(n_{H_2SO_4}=n_{H_2}=0,7\left(mol\right)\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,7}{0,5}=1,4\left(M\right)\)

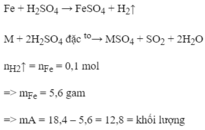


Có đúng ko bạn ơi