Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt nZn = x (mol) và nCu = 2x (mol)
(Vì hỗn hợp bột gồm Zn và Cu có tỉ lệ về số mol là 1:2)
⇒ mhỗn hợp = mZn + mCu
= 65x + 64 × 2x) = 19,3 g
⇒ x = 0,1 mol
Có nFe3+ = 0,4 mol. Xảy ra các quá trình sau:
PTHH: Zn + 2Fe3+ → Zn2+ + 2Fe2+
TPT: 1mol 2mol
TĐB: 0,1 → ?(mol)
=>nFe3+ = 0,1.2110,1.2 = 0,2(mol)
PTHH: Cu + 2Fe3+ → Cu2+ + 2Fe2+
TPT: 1mol 2mol
TĐB: ?(mol) ← 0,2(mol)
=> nCu= 0,2.12=0,1(���)20,2.1=0,1(mol)
⇒ m = mCu dư = 0,1 × 64 = 6,4 g
tick giúp tớ, cảm ơn bạn
Theo đề gọi \(n_{Zn}=x\left(mol\right),n_{Cu}=2x\left(mol\right)\)
Có:
\(m_{Zn}+m_{Cu}=19,3\\ \Leftrightarrow65x+64.2x=19,3\\ \Rightarrow x=0,1\)
=> Dung dịch sau \(\left\{{}\begin{matrix}SO_4^{2-}=0,6\\Fe^{2+}=0,4\\Zn^{2+}=0,1\\Cu^{2+}=0,1\end{matrix}\right.\)
\(\Rightarrow m_{kim.loại}=m_{Cu}=0,1.64=6,4\left(g\right)\)

Đặt nZn = x (mol) và nCu = 2x (mol)
(Vì hỗn hợp bột gồm Zn và Cu có tỉ lệ về số mol là 1:2)
⇒ mhỗn hợp = mZn + mCu
= 65x + 64 × 2x) = 19,3 g
⇒ x = 0,1 mol
Có nFe3+ = 0,4 mol. Xảy ra các quá trình sau:
PTHH: Zn + 2Fe3+ → Zn2+ + 2Fe2+
TPT: 1mol 2mol
TĐB: 0,1 → ?(mol)
=>nFe3+ = \(\dfrac{0,1.2}{1}\) = 0,2(mol)
PTHH: Cu + 2Fe3+ → Cu2+ + 2Fe2+
TPT: 1mol 2mol
TĐB: ?(mol) ← 0,2(mol)
=> nCu= \(\dfrac{0,2.1}{2}=0,1\left(mol\right)\)
⇒ m = mCu dư = 0,1 × 64 = 6,4 g

Đáp án A
n H 2 = 8 , 96 22 , 4 = 0 , 4 mol
Gọi số mol Na là a mol => số mol của Al là 2a mol
m gam chất rắn không tan là Al => Al dư sau phản ứng với NaOH
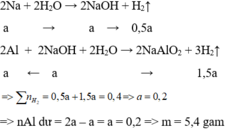

a) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_M=a\left(mol\right)\\n_{Al}=2a\left(mol\right)\end{matrix}\right.\)
=> a.MM + 54a = 15,6 (1)
\(n_{Cl_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
M0 - 2e --> M+2
a--->2a
Al0 - 3e --> Al+3
2a-->6a
Cl20 + 2e --> 2Cl-1
0,6-->1,2
2H+1 + 2e --> H20
0,4<--0,2
Bảo toàn e: 2a + 6a = 1,6
=> a = 0,2
Thay vào (1) => MM = 24 (g/mol)
=> M là Mg
b) Xét \(m_{Mg}+m_{Al}=0,1.24+0,2.27=7,8\left(g\right)\)
=> Không có khí thoát ra
=> pư tạo ra sản phẩm khử là NH4NO3
PTHH: 4Mg + 10HNO3 --> 4Mg(NO3)2 + NH4NO3 + 3H2O
0,1---->0,25
8Al + 30HNO3 --> 8Al(NO3)3 + 3NH4NO3 + 9H2O
0,2--->0,75
=> nHNO3 = 0,25 + 0,75 = 1 (mol)

Gọi \(n_{Fe_3O_4}=a\left(mol\right)\rightarrow n_{Cu}=3a\left(mol\right)\)
\(232a+64.3a=21,2\\ \Leftrightarrow a=0,05\left(mol\right)\)
\(m_{HCl}=125.14,6\%=18,25\left(g\right)\)
PTHH:
Fe3O4 + 8HCl ---> FeCl2 + 2FeCl3 + 4H2O
0,05------>0,4------->0,05---->0,1
\(m_X=0,05.3.64=9,6\left(g\right)\)
\(m_{dd}=232.0,05+125=136,6\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{0,05.127}{136,6}.100\%=4,65\%\\C\%_{FeCl_3}=\dfrac{0,1.162,5}{136,6}.100\%=11,9\%\\C\%_{HCl\left(dư\right)}=\dfrac{18,25-0,4.36,5}{136,6}=2,67\%\end{matrix}\right.\)


\(3Zn+Fe_2\left(SO_4\right)_3\rightarrow3ZnSO_4+2Fe\)
x -------------0,2---------------------------\(\dfrac{2x}{3}\) (mol)
\(3Cu+Fe_2\left(SO_4\right)_3\rightarrow3CuSO_4+2Fe\)
2x -----------0,2------------------------------\(\dfrac{4x}{3}\) (mol)
Gọi x(mol) là số mol của Zn và Fe
Theo đề bài ta có:
\(m_{Zn}+m_{Cu}=m_{hh}\)
⇔ 65 . x + 64 . 2x = 19,3
⇔ x = 0,1(mol)
⇒ \(\left\{{}\begin{matrix}n_{Zn}=0,1\left(mol\right)\\n_{Cu}=0,2\left(mol\right)\end{matrix}\right.\)
\(n_{Fe}=\dfrac{2x}{3}+\dfrac{4x}{3}=\dfrac{2.0,1}{3}+\dfrac{4.0,2}{3}=0,33\left(mol\right)\)
\(m_{Fe}=n.M=0,33.56=18,48\left(g\right)\)
\(m_{Fe_2\left(SO_4\right)_3}=n.M=0,2.400=80\left(g\right)\)
Ta có: \(m_{hh}+m_{Fe_3\left(SO_4\right)_3}=m_{kl}+m_{Fe}\)
⇔ \(m_{kl}\) = 19,3 + 80 - 18,48 = 80,82(g)
Cam on bn nha