đốt cháy hoàn toàn m gam cacbon trong V lít khí Oxi (đktc) thu được hỗn hợp khí A có tỉ khối đối với oxi là 1,25
a. hãy xác định thành phần % theo thể tích các khí có trong hỗn hợp A
b. tính m và V.biết rằng khi dẫn hỗn hợp khí A vào bình đựng dunh dịch Ca(OH)2 dư tạo thành 6 gam kết tủa trắng


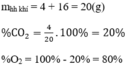

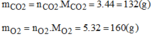
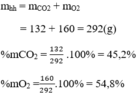
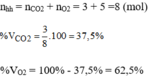
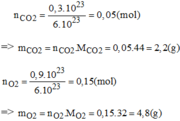
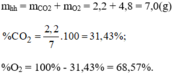
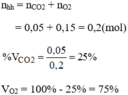

a)
dA/O\(_2\) = \(\dfrac{M_A}{32}\) = 1,25 \(\Rightarrow\) MA = 32 . 1,25 = 40
PTPƯ: C + O2 -----> CO2
C + CO2 -----> 2CO
Trường hợp 1 (Oxi dư)
Ta có: MA = \(\dfrac{44x+\left(1-x\right).32}{1}\) = 40 \(\Rightarrow\) x = \(\dfrac{2}{3}\)
Vậy %VCO\(_2\) = \(\dfrac{2}{3}\) . 100 = 66,67%
%VO\(_2\) = 33,33%
Trường hợp 2 (Oxi thiếu)
MA = \(\dfrac{44x+\left(1-x\right).28}{1}\) = 40 \(\Rightarrow\) x = 0,75
Vậy % VCO\(_2\) = \(\dfrac{a}{a+b}\) . 100 = \(\dfrac{3b}{4b}\) . 100 = 75%
%VCO = 25%
b)
CO2 + CA(OH)2 -----> CaOH3 \(\downarrow\) + H2O
0,06 \(\leftarrow\) 0,06 = \(\dfrac{6}{100}\)
Trường hợp 1 (nCO\(_2\) = 0,06 mol \(\Rightarrow\) nO\(_2\) dư = 0,03 mol)
Vậy mc = 0,06.12 = 0,75 (g)
VO\(_2\) = (0,06 + 0,03) . 22,4 = 2,016 (l)
Trường hợp 2 (nCO\(_2\) = 0,06 mol, nCO = \(\dfrac{1}{3}\) nCO\(_2\) = 0,02 mol)
\(\Rightarrow\) nC = nCO\(_2\) + nCO = 0,06 + 0,02 = 0,08 (mol)
\(\Rightarrow\) mC = 0,08 . 12 = 0,96 (g)
nO\(_2\) = nCO\(_2\) + \(\dfrac{1}{2}\) nCO = 0,06 + 0,01 = 0,07 (mol)
VO\(_2\) = 0,07.22,4 = 1,568 (l)
cho mình hỏi tại sao ở câu b th 1 no2 dư = 0,03 với còn th 2 thì nco = 1/3 nco2