Bài 8: Hòa tan muối RCO3 trong lượng vừa đủ dung dịch HNO3 20% thu được dung dịch có nồng độ muối là 26,582%. Tìm CTHH của muối cacbonat đã dùng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


gọi công thức của muối đó là M2(CO3)x với x là hóa trị của kim loại đó
gọi a là số mol của muối đó
M2(CO3)x + xH2SO4 ---> M2(SO4)x + xH2O + xCO2
a mol --- --- ->ax mol --- -->a mol --- --- --- --- --->ax mol
khối lượng H2SO4 tham gia phản ứng là 98ax gam
=> khối lượng dd H2SO4 là 1000ax gam
khối lượng muối cacbonat là a(2M + 60x) gam
khối lượng muối sunfat là a(2M + 96x) gam
khối lượng khí CO2 bay ra là 44ax gam
theo định luật bảo toàn khối lượng, ta có:
khối lượng dd sau phản ứng là
m = a(2M + 60x) + 1000ax - 44ax = 2aM + 1016ax
theo đề ta có:
(2aM + 96ax)/(2aM + 1016ax) = 14,18/100
triệt tiêu a ở vế trái, quy đồng 2 vế rồi biến đổi ta tính được:
M = 28x
kim loại chỉ có 3 hóa trị từ 1 đến 3
ta thay x lần lượt bằng 1, 2, 3 thì ra được kết quả thích hợp là:
x = 2 và M = 56
=> kim loại đó là Fe
=> khối lượng dd H2SO4 là 1000ax gam
cho mình hỏi làm sao suy ra được???![]()

Giả sử có 1 mol RCO3
PTHH: RCO3 + 2HCl → RCl2 + CO2↑ + H2O
1 → 2 1 1 1 (mol)
Ta có mdd(sau pứ) = mRCO3+mdd(HCl)−mCO2
⟹ mdd(sau pứ) = \(\dfrac{\text{MR+60+(2.36,5.100%)}}{7,3\%-1,44}\)=MR+1016
⟹ C%(RCl2)=mRCl2mdd(sau).100%=\(\dfrac{M_{R_{ }}+71}{_{ }M_R+1016}\).100%=9,135%
⟹ MR = 24 (Mg)
Vậy công thức của muối là MgCO3.

gọi công thức muối là ACO3
n CO2=0,448:22,4=0,02mol
PTHH: ACO3+2HCl=>ACl2+CO2+H2O
0,02<--0,04<-0,02<-0,02->0,02
=> mHCl=0,04.36,5=1,46g
=> mddHCl=\(\frac{1,46}{10}.100=14,6g\)
ta có MACO3=2:0,02=100g/mol
=> M A=100-12-16.3=40
=> A là Ca
=> công thức muois là CACO3
ta có m CaCl2=0,02.111=2,22g
=> mddCaCl2=2+14,6-0,02.44-0,02.18=15,36g
=> C% CaCl2=2,22:15,36.100=14,45%

Gọi CTHH của muối cacbonat là MCO3
MCO3 + H2SO4 → MSO4 + CO2 + H2O
Gọi x là số mol của MCO3
\(\Rightarrow m_{MCO_3}=xM_M+60x\left(g\right)\)
Theo PT: \(n_{H_2SO_4}=n_{MCO_3}=x\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=98x\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\frac{98x}{20\%}=490x\left(g\right)\)
Theo PT: \(n_{CO_2}=n_{MCO_3}=x\left(mol\right)\)
\(\Rightarrow m_{CO_2}=44x\left(g\right)\)
Ta có: \(m_{dd}saupứ=xM_M+60x+490x-44x=xM_M+506x\left(g\right)\)
Theo PT: \(n_{MSO_4}=n_{MCO_3}=x\left(mol\right)\)
\(\Rightarrow m_{MSO_4}=xM_M+96x\left(g\right)\)
\(C\%_{MSO_4}=\frac{xM_M+96x}{xM_M+506x}\times100\%=24,91\%\)
\(\Leftrightarrow\frac{M_M+96}{M_M+506}=0,2491\)
\(\Rightarrow M_M+96=0,2491M_M+126,0446\)
\(\Leftrightarrow0,7509M_M=30,0446\)
\(\Leftrightarrow M_M=40\left(g\right)\)
Vậy M là Canxi Ca
CTHH của muối cacbonat là CaCO3
Gọi: CTHH của muối cacbonat là : MCO3 ( x mol )
MCO3 + H2SO4 --> MSO4 + CO2 + H2O
x________x_________x______x
mMCO3 = x ( M +60 ) (g)
mH2SO4 = 98x g
mdd H2SO4 = 98x*100/20=490x (g)
mCO2 = 44x g
mdd sau phản ứng = x(M+60) + 490x - 44x = x ( M+506) (g)
mMSO4 = x ( M + 96 ) (g)
Ta có : \(C\%MSO_4=\frac{x\left(M+96\right)}{x\left(M+506\right)}\cdot100\%=24.91\%\)
\(\Leftrightarrow M+96=0.2491\left(M+506\right)\)
\(\Leftrightarrow M+96=0.2491M+126.0446\)
\(\Leftrightarrow0.7509M=30.0446\)
\(\Leftrightarrow M\approx40\left(Ca\right)\)
Vậy: CTHH của muối cacbonat là : CaCO3

tham khảo
Coi mdd H2SO4=100(gam)mdd H2SO4=100(gam)
⇒nH2SO4=100.9,8%98=0,1(mol)⇒nH2SO4=100.9,8%98=0,1(mol)
Gọi CTHH của muối cacbonat kim loại R hóa trị n là R2(CO3)nR2(CO3)n
R2(CO3)n+nH2SO4→R2(SO4)n+nCO2+nH2OR2(CO3)n+nH2SO4→R2(SO4)n+nCO2+nH2O
Theo phương trình ,ta có :
nCO2=nH2SO4=0,1(mol)nCO2=nH2SO4=0,1(mol)
nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)
Sau phản ứng ,
mdd=0,1n(2R+60n)+100−0,1.44=0,2Rn+101,6(gam)mdd=0,1n(2R+60n)+100−0,1.44=0,2Rn+101,6(gam)
mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)
⇒C%muối=(0,2Rn+9,6):(0,2Rn+101,6).100%=14,18%⇒C%muối=(0,2Rn+9,6):(0,2Rn+101,6).100%=14,18%
⇒R=28n⇒R=28n
Với n=1n=1 thì R=28R=28(loại)
Với n=2n=2 thì R=56(Fe)R=56(Fe)
Với n=3n=3 thì R=84R=84(loại)
Vậy kim loại R hóa trị n là FeFe hóa trị II

\(a.Mg+2HCl->MgCl_2+H_2\\ Fe+2HCl->FeCl_2+H_2\\ b.Giả.sử:có:100g.dd.HCl\\ n_{HCl}=\dfrac{20\%.100}{36,5}=\dfrac{40}{73}mol\\ n_{Fe}=a;n_{Mg}=b\\ 2a+2b=\dfrac{40}{73}\\ BTKL:m_{ddsau}=56a+24b+100-2\left(a+b\right)=54a+22b+100\left(g\right)\\ C\%_{MgCl_2}=\dfrac{95b}{54a+22b+100}=\dfrac{11,787}{100}\\ -54a+783,97b=100\\ a=b=0,137\left(mol\right)\\ C\%FeCl_2=\dfrac{0,137\cdot127}{\dfrac{95\cdot0,137}{11,787\%}}\cdot100\%=15,757\%\)

Đặt nFe = x,nZn = y.
Khối lượng dung dịch sau phản ứng là 56x+65y+980(x+y) - 2(x+y) = 1034x+1043y
%khối lượng muối sắt = 152x/(1034x+1043y)
=> y=2x
=> % khối lượng muối kẽm = 161y/(1034x+1043y) = 10,32%
=> Đáp án A
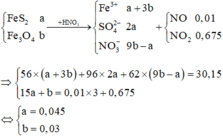
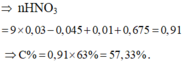
Giả sử số mol RCO3 phản ứng là 1 mol
\(RCO_3+2HNO_3\rightarrow R\left(NO_3\right)_2+H_2O+CO_2\)
1.....................2.....................1...................1...............1
=> \(m_{ddsaupu}=R+60+\dfrac{2.63}{20\%}-1.44=R+646\left(g\right)\)
\(C\%_{R\left(NO_3\right)_2}=\dfrac{R+62.2}{R+646}.100=26,582\)
=> R=65 (Zn)
=> CT muối cacbonat : ZnCO3