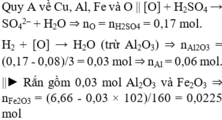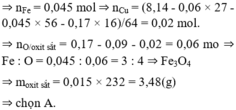Cho $8,14$ gam hỗn hợp A gồm $CuO$, $Al_{2}O_{3}$, $Fe_{x}O_{y}$. Cho $H_{2}$ dư đi qua A nung nóng thu được $1,44$ gam $H_{2}O$. Hòa tan hoàn toàn A cần vừa đủ $170$ml dung dịch $H_{2}SO_{4}$ $1M$ được dung dịch B. Cho B+ $NaOH_{dư}$ thu được kết tủa. Nung kết tủa trong không khí đến khối lượng không đổi thì thu được $5,2$ gam chất rắn. Tìm công thức của oxit sắt.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4(l) ---> FeSO4 + H2
0,1<-------------------------------0,1
\(m_{Fe}=0,1.56=5,6\left(g\right)\\ n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH:
2Fe + 6H2SO4(đ,n) ---> Fe2(SO4)3 + 3SO2 + 6H2O
0,1-------------------------------------------->0,15
2Ag + 2H2SO4(đ,n) ---> Ag2SO4 + SO2 + 2H2O
0,2<----------------------------------------0,1
=> mAg = 0,2.108 = 21,6 (g)
=> \(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{5,6+21,6}.100\%=20,44\%\\\%m_{Ag}=100\%-20,44\%=79,56\%\end{matrix}\right.\)
b) nNaOH = 0,25.1,5 = 0,375 (mol)
\(T=\dfrac{0,375}{0,25}=1,5\) => Tạo cả 2 muối
PTHH:
2NaOH + SO2 ---> Na2SO3 + H2O
0,375--->0,1875--->0,1875
Na2SO3 + SO2 + H2O ---> 2NaHSO3
0,0625<---0,0625----------->0,125
=> \(\left\{{}\begin{matrix}C_{M\left(Na_2SO_3\right)}=\dfrac{0,1875-0,0625}{0,25}=0,48M\\C_{M\left(NaHSO_3\right)}=\dfrac{0,125}{0,25}=0,5M\end{matrix}\right.\)

Chọn đáp án A
Quy A về Cu, Al, Fe và O || [O] + H2SO4 → SO42– + H2O ⇒ nO = nH2SO4 = 0,17 mol.
H2 + [O] → H2O (trừ Al2O3) ⇒ nAl2O3 = (0,17 - 0,08)/3 = 0,03 mol ⇒ nAl = 0,06 mol.
||► Rắn gồm 0,03 mol Al2O3 và Fe2O3 ⇒ nFe2O3 = (6,66 - 0,03 × 102)/160 = 0,0225 mol
⇒ nFe = 0,045 mol ⇒ nCu = (8,14 - 0,06 × 27 - 0,045 × 56 - 0,17 × 16)/64 = 0,02 mol.
⇒ nO/oxit sắt = 0,17 - 0,09 - 0,02 = 0,06 mo ⇒ Fe : O = 0,045 : 0,06 = 3 : 4 ⇒ Fe3O4
⇒ moxit sắt = 0,015 × 232 = 3,48(g) ⇒ chọn A.

Fe có hóa trị II và III khi liên kết với O hóa trị II thì có thể tạo được FeO, Fe2O3, Fe3O4
=> CÔNG THỨC: FeO2 và Fe2O4 sai
Gỉa sử FexOy là Fe3O4, thì ta có PTHH:
\(Fe_3O_4+4H_2SO_4--->FeSO_4+Fe_2(SO_4)_3+4H_2O\)
Khác so với sơ đồ phản ứng đề ra
=> Công thức Fe3O4 loại
Vậy FexOy đó phải là Fe2O3
\(Fe_2O_3+3H_2SO_4--->Fe_2(SO_4)_3+3H_2O\)
Chon B. 2 và 3

Gọi \(\left\{{}\begin{matrix}n_{RO}=2x\\n_{Fe_2O_3}=x\end{matrix}\right.\)
Theo đề:
\(R.2x+56.2x=31,56\)
\(\Rightarrow2x.R=31,56-112x\)
Mặt khác: \(2x.\left(R+16\right)+160x=36,36\)
\(\Leftrightarrow2xR+32x+160x=36,6\Leftrightarrow31,56-112x+32x+160x=36,36\)
=> x = 0,06
\(\Rightarrow R=\dfrac{31,56-112.0,06}{2.0,06}=207\)
Vậy kim loại R là Pb (chì).