Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
► Xét phần 1: Y + NaOH → H2. Mặt khác, phản ứng xảy ra hoàn toàn ⇒ Al dư.
nAl dư = 0,15 ÷ 1,5 = 0,1 mol. Phần không tan T là Fe ⇒ nFe = nH2 = 0,45 mol.
Lần lượt bảo toàn nguyên tố Oxi và Fe ⇒ nAl2O3 = 0,2 mol.
● GIẢ SỬ phần 1 tác dụng với HCl thì nH2 = 0,1 × 1,5 + 0,45 = 0,6 mol.
||⇒ phần 2 gấp 1,2 ÷ 0,6 = 2 lần phần 1 ⇒ lượng ban đầu gấp 3 lần phần 1.
► m = 3 × (0,1 × 27 + 0,2 × 102 + 0,45 × 56) = 144,9(g) ⇒ chọn B.

Chọn đáp án D
Xét phần 1: do sinh ra H2 ⇒ Al dư. nH2 = 0,075 mol ⇒ nAl dư = 0,05 mol.
Rắn không tan là Fe. Ta có: 2H2SO4 + 2e → SO2 + SO42– + 2H2O.
⇒ nSO42– = nSO2 = 0,6 mol ⇒ nFe = (82,8 – 0,6 × 96) ÷ 56 = 0,45 mol.
8Al + 3Fe3O4 → 4Al2O3 + 9Fe ⇒ nAl2O3 = 0,45 × 4 ÷ 9 = 0,2 mol.
⇒ mphần 1 = 0,05 × 27 + 0,2 × 102 + 0,45 × 56 = 46,95(g) ⇒ m phần 2 = 187,8(g).
⇒ phần 2 gấp 4 lần phần 1 ⇒ phần 2 chứa 0,2 mol Al; 0,8 mol Al2O3; 1,8 mol Fe.
Ta có: nH+ = 4nNO + 2nNO2 + 2nO + 10nNH4+ ⇒ nNH4+ = 0,015 mol.
Đặt nFe(NO3)2 = b ⇒ a + b = nFe = 1,8 mol; Bảo toàn electron:
0,2 × 3 + 3a + 2b = 1,25 × 3 + 1,51 + 0,015 × 8. Giải hệ có: a = 1,18


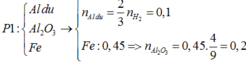
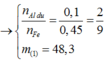
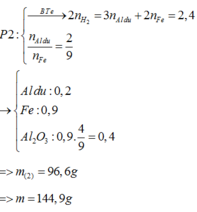

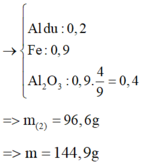





Đáp án B