Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2Al + 3CuSO4 = Al2(SO4)3 + 3Cu.
Cứ 54 gam nhôm phản ứng tạo ra 192 gam Cu làm khối lượng thanh nhôm tăng lên 138 gam.
Khối lượng thanh nhôm của bạn chỉ tăng 1,38 gam tức là chỉ có 1,92 gam đồng thoát ra.

nAgNO3= 0,1 (mol)
Al + 3AgNO3 \(\rightarrow\) Al(NO3)3 + 3Ag
Cứ 1 mol Al pư thì khối lượng thanh Al tăng 297 g
0,01 mol <--------------------------------------- (52,97 - 50)
a) mAl pư = 0,01 . 27=,27 (g)
Theo pt nAg = 3nAl=3 . 0,01 = 0,03 (mol) = nAgNO3 pư
mAg=0,03 . 108 = 3,24 (g)
b)nAgNO3 dư = 0,1 - 0,03 = 0,07 (mol)
CM (AgNO3)= \(\frac{0,07}{0,25}\) = 0,28 (M)
CM (Al(NO3)3) = \(\frac{0,01}{0,25}\) = 0,04 (M)

Al: 25 gam + 0,1 mol CuSO4 → thanh nhôm nặng 25,69 gam.
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Sau phản ứng mtăng = 25,69 - 25 = 0,69 gam
=> \(n_{Al} = 2. \dfrac{0,69}{3 .64 - 2 . 27} = 0,01 mol\)
=> nAl2(SO4)3 = 0,005 mol; nCuSO4dư = 0,1 - 0,015 = 0,085 mol
=> CM Al2(SO4)3= 0,025 M; CM CuSO4 = 0,425 M

a, PT: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
Gọi nFe (pư) = x (mol) ⇒ nCu = nFe = x (mol)
Ta có: m tăng = mCu - mFe (pư)
⇒ 1,2 = 64x - 56x ⇒ x = 0,15 (mol)
⇒ mCu = 0,15.64 = 9,6 (g)
b, Ta có: \(m_{CuSO_4}=400.10\%=40\left(g\right)\Rightarrow n_{CuSO_4}=\dfrac{40}{160}=0,25\left(mol\right)\)
Theo PT: \(n_{FeSO_4}=n_{CuSO_4\left(pư\right)}=n_{Fe}=n_{Cu}=0,15\left(mol\right)\)
⇒ nCuSO4 (dư) = 0,25 - 0,15 = 0,1 (mol)
Có: m dd sau pư = mFe + m dd CuSO4 - mCu = 0,15.56 + 400 - 9,6 = 398,8 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{0,15.152}{398,8}.100\%\approx5,72\%\\C\%_{CuSO_4\left(dư\right)}=\dfrac{0,1.160}{398,8}.100\%\approx4,01\%\end{matrix}\right.\)

PTHH: \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
x__________________x_______2x (mol)
Giả sử lượng Bạc bám hết vào thanh đồng
Ta có: \(3-64x+108\cdot2x=4,21\) \(\Rightarrow x\approx0,008\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Cu\left(p/ứ\right)}=n_{Cu\left(NO_3\right)_2}=0,008\left(mol\right)\\n_{Ag}=0,016\left(mol\right)\\\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Cu\left(p/ứ\right)}=0,008\cdot64=0,512\left(g\right)\\m_{Ag}=0,016\cdot108=1,728\left(g\right)\\m_{Cu\left(dư\right)}=2,488\left(g\right)\\m_{Cu\left(NO_3\right)_2}=0,008\cdot188=1,504\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd\left(sau.p/ứ\right)}=m_{Cu\left(ban.đầu\right)}+m_{ddAgNO_3}-m_{Ag}-m_{Cu\left(dư\right)}=228,784\left(g\right)\)
\(\Rightarrow C\%_{Cu\left(NO_3\right)_2}=\dfrac{1,504}{228,784}\cdot100\%\approx0,66\%\)

HD:
Fe + CuSO4 ---> FeSO4 + Cu
x x mol x x
a) Khối lượng Fe tăng lên = mCu (thoát ra) - mFe (tan vào dd) ---> 4%.50 = 64.x - 56x ---> x = 0,25 mol.
---> mCu = 64x = 64.0,25 = 16 gam.
b) [FeSO4] = 0,25/0,4 = 0,625 M; [CuSO4] = (0,4 - 0,25)/0,4 = 0,375 M.

n C u S O 4 = 0,5.0,2 = 0,1 mol
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
2x……3x……..x……3x (Mol)
Theo bài ta có:
m C u b á m v à o - m A l tan = m A l t ă n g
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
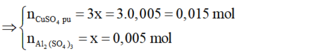

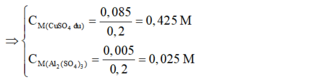
⇒ Chọn D.



mk nghĩ bn nên đăng vào buổi tối sẽ nhìu người giải hơn sáng sớm thế này, nếu bn đăng bài này vào tối quá thì mk đã giải cho rùi, h sắp đi hok mất tiu rùi
khi nào rãnh bn giải hộ mk nhé