Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nHgO = 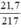 = 0,1 mol.
= 0,1 mol.
Phương trình hóa học của phản ứng khử HgO:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1 .201 = 20,1g.
nH2 = 0,1 mol.
VH2 = 0,1 .22,4 =2,24l.

HgO+H2-to>Hg+H2O
0,025-0,025--0,025
n HgO=\(\dfrac{8,68}{217}\)=0,04 mol
n H2=\(\dfrac{0,56}{22,4}\)=0,025 mol
=>HgO dư
=>m Hg=0,025.201=5,025g
nH2 = 0,56/22,4 = 0,025 (mol)
nHgO = 8,68/217 = 0,04 (mol)
PTHH: HgO + H2 -> (t°) Hg + H2O
LTL: 0,025 < 0,04 => H2 dư
nH2 (p/ư) = nHg = 0,025 (mol)
VH2 = (0,04 - 0,025) . 22,4 = 0,336 (l)
mHg = 0,025 . 201 = 5,025 (g)

\(n_{HgO}=\dfrac{43,4}{217}=0,2\left(mol\right)\)
PTHH: HgO + H2 --to--> Hg + H2O
0,2 0,2 0,2
\(\rightarrow\left\{{}\begin{matrix}m_{Hg}=201.0,2=40,2\left(g\right)\\V_{H_2}=0,2.22,4=4,48\left(l\right)\end{matrix}\right.\)
nHgO = 43,4 : 217 = 0,2 (mol)
pthh : HgO + H2 -t> Hg + H2O
0,2 0,2 0,2
mHg = 0,2 . 201 = 40,2 (G)
VH2 = 0,2 . 22,4 = 4,48 (L)

2HgO -t--> 2Hg + O2
0,15-------------->0,75 (mol)
=> mO2 = 0,75 . 32 = 24 (g)

nHgO = 21,7 : 217 = 0,1 (mol)
pthh : HgO + H2 -t--> H2O + Hg
0,1---->0,1--------------->0,1 (MOL)
=> mHg = 0,1 . 201 = 20,1 (G)
=> VH2 = 0,1 . 22,4 = 2,24 (L)

3.
nHgO = 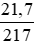
Phương trình hóa học của phản ứng khử HgO:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1 .201 = 20,1g.
nH2 = 0,1 mol.
VH2 = 0,1 .22,4 =2,24l.
1.
Phương trình phản ứng:
Fe3O4 + 4H2 → 4H2O + 3Fe
HgO + H2 → H2O + Hg
PbO + H2 → H2O + Pb

Bài 1:
\(PTHH:2HgO\underrightarrow{Phân.hủy}2Hg+O_2\\ á,Theo.PTHH:n_{O_2}=\dfrac{1}{2}.n_{HgO}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\\ V_{O_2\left(đktc\right)}=n.22,4=0,05.22,4=1,12\left(l\right)\)
\(b,n_{HgO}=\dfrac{m}{M}=\dfrac{43,4}{217}=0,2\left(mol\right)\\ Theo.PTHH:n_{Hg}=n_{HgO}=0,2\left(mol\right)\\ m_{Hg}=n.M=0,2.201=40,2\left(g\right)\)
\(c,n_{Hg}=\dfrac{m}{M}=\dfrac{14,07}{201}=0,07\left(mol\right)\\ Theo.PTHH:n_{HgO}=n_{Hg}=0,07\left(mol\right)\\ m_{HgO}=n.M=0,07.217=15,19\left(g\right)\)
Câu 2:
\(a,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ Theo.PTHH:n_{Zn}=n_{H_2}=0,3\left(mol\right)\\ m_{Zn}=n.M=0,3.65=19,5\left(g\right)\\ b,Theo.PTHH:n_{HCl}=2.n_{Zn}=2.0,3=0,6\left(mol\right)\\ m_{HCl}=n.M=0,6.36,5=21,9\left(g\right)\)

a. Số mol thủy ngân (II) oxit là: n = \(\frac{m}{M}\) = \(\frac{21,7}{217}\) = 0,1 (mol)
phương trình phản ứng:
HgO + H2 → H2O + Hg
1 mol 1 mol 1mol 1 mol
0,1 0,1 0,1 0,1
Khối lượng thủy ngân thu được: m = 0,1.201 = 20,1 (g)
b. Số mol khí hi đro: n = 0,1 mol
Thể tích khí hiđro cần dùng ở đktc là:
V = 22,4.0,1 = 2,24 (lít)
a/ PTHH: HgO + H2 ===> Hg + H2O
nHgO = 21,7 / 217 = 0,1 mol
=> nHg = nHgO = 0,1 mol
=> mHg = 0,1 x 201 = 20,1 gam
b/ Theo phương trình, ta có:
nH2 = nHgO = 0,1 mol
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít

\(HgO\left(0,1\right)+H_2\left(0,1\right)\rightarrow Hg\left(0,1\right)+H_2O\)
Ta có: \(n_{HgO}=\dfrac{21,7}{217}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Hg}=0,1.201=20,1\left(g\right)\\m_{H_2}=0,1.2=0,2\left(g\right)\end{matrix}\right.\)
a. Số mol thủy ngân (II) oxit là: n = =
= 0,1 (mol)
phương trình phản ứng:
HgO + H2 → H2O + Hg
1 mol 1 mol 1mol 1 mol
0,1 0,1 0,1 0,1
Khối lượng thủy ngân thu được: m = 0,1.201 = 20,1 (g)
b. Số mol khí hi đro: n = 0,1 mol
Thể tích khí hiđro cần dùng ở đktc là:
V = 22,4.0,1 = 2,24 (lít)


PTHH: HgO + \(H_2\) ---> Hg + \(H_2O\)
0,1 mol 0,1 mol 0,1 mol 0,1 mol
+ Số mol của HgO:
\(n_{HgO}\) = \(\dfrac{m}{M}\) = \(\dfrac{21,7}{217}\) = 0,1 (mol)
+ Số g thủy ngân (Hg) thu được:
\(m_{Hg}\) = n . M = 0,1 . 201 = 20,1 (g)
Vậy: thu được 20,1 g Hg (thủy ngân)
\(n_{HgO}=\dfrac{m_{HgO}}{M_{HgO}}=\dfrac{21,7}{217}=0,1\left(mol\right)\)
\(HgO+H_2\underrightarrow{t^0}H_2O+Hg\)
Theo PT: 1mol _ 1mol _ 1mol _ 1mol
Theo đề: 0,1 mol _ 0,1 mol _ 0,1 mol _ 0,1 mol
\(m_{Hg}=n_{Hg}.M_{Hg}=0,1.201=20,1\left(g\right)\)