Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Do các chất đều đơn chức ⇒ muối có dạng RCOONa với số mol là 0,1.
Bảo toàn nguyên tố hiđro
⇒ số H/muối = 0,05 × 2 ÷ 0,1 = 1 ⇒ R là H.
+ Bảo toàn khối lượng: mX + mNaOH = mmuối + mancol + mH2O ⇒ nH2O = 0,01 mol.
⇒ naxit = 0,01 mol ⇒ neste = 0,09 mol ⇒ nancol > neste = 0,09 mol.
⇒ Mancol < 3,2 ÷ 0,09 = 35,56 ⇒ ancol là CH3OH ⇒ este là HCOOCH3.
⇒ %meste = 0,09 × 60 ÷ 6,18 × 100% = 87,38%

Đáp án D
nNaOH = 0,1 mol
⇒ nMuối = nRCOONa = 0,1 mol.
+ Đốt cháy 0,1 mol RCOONa
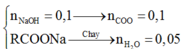
⇒ nH2O = 0,05 mol ⇒ nH = 0,1 mol
⇒ Muối là HCOONa.
Sơ đồ ta có.
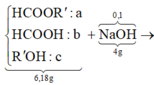
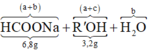
+ Dễ dàng tính được mH2O = 0,18 gam
⇒ nH2O = 0,01 mol
⇒ nHCOOR' = 0,1 – 0,01 = 0,09 mol.
+ Ta có
nAncol = a + c = (0,09 + c) > 0,09
⇒ MAncol < 3,2÷0,09 = 35,67
⇒ Ancol là CH3OH
⇒ Este là HCOOCH3 với số mol = 0,09
⇒ mHCOOCH3 = 5,4 gam
⇒%mHCOOCH3 = 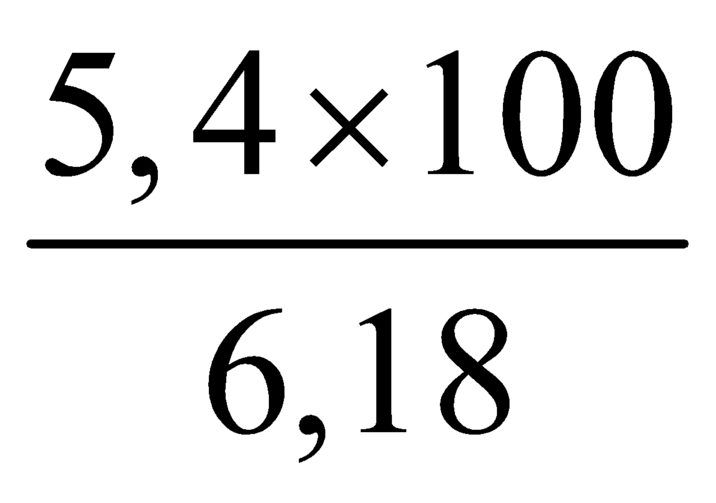 ×100% = 87,38%
×100% = 87,38%

Đáp án C
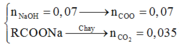
Bảo toàn nguyên tố Natri → nNa2CO3 = 0,09 mol.
Este và axit đơn → nmuối = nNaOH = 0,18 mol.
∑nC = nNa2CO3 + nCO2 = 0,09 + 0,09 = 0,18 mol → muối chứa 1 C.
⇒ muối là HCOONa: 0,18 mol. Bảo toàn khối lượng:
nH2O = (11,16 + 0,18 × 40 - 5,76 - 0,18 × 68) ÷ 18 = 0,02 mol = naxit
→ neste = 0,18 – 0,02 = 0,16 mol. Do ancol sau phản ứng gồm trong cả este và ancol tự do
⇒ sau phản ứng, số mol ancol > 0,16 mol ⇒ Mancol < 5,76 ÷ 0,16 = 36
⇒ ancol là CH3OH → số mol ancol sau phản ứng là 0,18 mol.
⇒ số mol ancol trong T là 0,18 – 0,16 = 0,02 mol
⇒ %nancol/T = 0,02 ÷ (0,02 + 0,16 + 0,02) × 100% = 10%.

Đáp án C
TQ : este : CnH2n+1COOCmH2m+1
Gọi số mol este ; axit ; ancol trong T lần lượt là a ; b ; c
=> nMuối = nNaOH = 0,18 mol
Muối khan :
CnH2n+1COONa + (n + 0,5)O2 -> 0,5Na2CO3 + (n + 0,5)CO2 + (n + 0,5)H2O
=> 0,18(n + 0,5) = 0,09 => n = 0
=> HCOONa
Bảo toàn khối lượng : mT + mNaOH = mmuối + mancol + mH2O
=> 11,16 + 40.0,18 = 0,18.68 + 5,76 + mH2O
=> nH2O = naxit = 0,02 mol => neste = nNaOH – naxit = 0,16 mol
=> nancol sau pứ = a + c = 0,16 + c > 0,16
=> Mancol < 5,76/0,16 = 36 => CH3OH
=> a + c = 0,18 mol => c = 0,02 mol
=> %nancol = 0,02/ (0,02 + 0,16 + 0,02) = 10%

Đáp án C
TQ : este : CnH2n+1COOCmH2m+1
Gọi số mol este ; axit ; ancol trong T lần lượt là a ; b ; c
=> nMuối = nNaOH = 0,18 mol
Muối khan : CnH2n+1COONa + (n + 0,5)O2 +0,5Na2CO3 + (n + 0,5)CO2 + (n + 0,5)H2O
Mol 0,18 0,09
=> 0,18(n + 0,5) = 0,09 => n = 0
=> HCOONa
Bảo toàn khối lượng : mT + mNaOH = mmuối + mancol + mH2O
=> 11,16 + 40.0,18 = 0,18.68 + 5,76 + mH2O
=> nH2O = naxit = 0,02 mol => neste = nNaOH – naxit = 0,16 mol
=> nancol sau pứ = a + c = 0,16 + c > 0,16
=> Mancol< 5,76/0,16 = 36 => CH3OH
=> a + c = 0,18 mol => c = 0,02 mol
=> %nancol = 0,02/ (0,02 + 0,16 + 0,02) = 10%


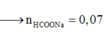



Vì M + NaOH → muối + 1 ancol
=> este ban đầu có gốc ancol cùng với ancol ban đầu
Đặt công thức của các chất trong M là: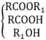
RCOOR1 + NaOH → RCOONa + R1OH
R2COOH + NaOH → R2COONa + H2O
Từ 2 PTHH trên => neste + naxit = nmuối = nNaOH = 0,15 (mol)
Đốt cháy 0,15 mol muối tạo ra 0,075 mol H2O => nH = 2nH2O = 0,15 (mol)
=> Số H có trong muối = nH/ nmuối = 0,15/0,15 = 1
=> Muối đó phải có công thức là HCOONa
=> Công thức của các chất trong M là: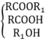
Sơ đồ: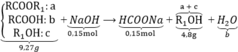
Bảo toàn khối lượng ta có: 9,27 + 0,15.40 = 0,15.68 + 4,8 + 18b
=> b = 0,015 (mol)
=> nHCOOH = nH2O = 0,015 (mol)
=> nHCOOR1 = 0,15 - 0,015 = 0,135 (mol)
Ta có: nR1OH = a + c = 0,135 +c > 0,135
=> MR1OH < 4,8 : 0,135 = 35,56
=> Ancol là CH3OH
=> Este là: HCOOCH3: 0,135 (mol)
%HCOOCH3 trong
M =
Đáp án cần chọn là: B