Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải chi tiết:
Gọi công thức chung của kim loại kiềm đó là X
X + HCl → XCl + 0,5H2
Theo PTHH: nX = 2nH2 = 0,2 mol
=> Li (M = 7) < MX = 3,8 : 0,2 = 19 < Na (M = 23)
Đáp án A

Đáp án B
Gọi công thức chung của hai kim loại kiềm là M .
Có phản ứng:
![]()
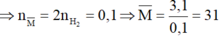
Do đó hỗn hợp cần có 1 kim loại có khối lượng mol nhỏ hơn 31 và 1 kim loại có khối lượng mol lớn hơn 31.
Mà hai kim loại kiềm thuộc hai chu kì liên tiếp
Nên hai kim loại kiềm trong hỗn hợp là Na và K.

Hoà tan hoàn toàn 6,2g hai kim loại kiềm ở 2 chu kì liên tiếp vào nước thu được H2 (đktc) và dung dịch X. Trung hòa ½ dung dịch X cần 100 ml dung dịch HCl 1M. Hai kim loại là
A. Li và Na B. Na và K C. K và Rb D. Rb và Cs
Gọi 2 kim loại cần tìm là R
\(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\)
\(ROH+HCl\rightarrow RCl+H_2O\)
Số mol của 1/2 dung dịch X : \(n_{ROH}=n_{HCl}=0,1\left(mol\right)\)
\(n_{R\left(bđ\right)}=n_{ROH}=0,2\left(mol\right)\)
=> \(M_R=\dfrac{6,2}{0,2}=31\)
Vì hai kim loại kiềm ở 2 chu kì liên tiếp
=> 2 kim loại cần tìm là Na và K
=> Chọn B

Bài 31:
Gọi CT chung của 2 kim loại nhóm IIA (kim loại X,Y) cần tìm là Z. (M(X)<M(Z)<M(Y))
Ta có: Z +2 HCl -> ZnCl2 + H2
nH2=0,672/22,4=0,03=nZ
=> 24<M(Z)=mZ/nZ= 1,67/0,03=35,667<40
=> M(Mg) < M(Z) < M(Ca)
=> X là Magie (Mg), Y là Canxi (Ca)
=> CHỌN B
Bài 33:
nH2=0,1(mol) => mH2=0,1.2=0,2(g)
Đặt CTHH chung của 2 kim loại kiềm là A.
PTHH: A + H2O -> AOH + 1/2 H2
nH2O=nH2.2=0,1.2=0,2(mol) => mH2O=3,6(g)
Theo ĐLBTKL ta có:
mA+ mH2O = mAOH + mH2
<=>mAOH=(mA+mH2O) - mH2= 6,2 + 3,6 - 0,2= 9,6(g)
=> m(rắn)=9,6(g)
=> CHỌN C

a) Gọi công thức chung của 2 kim loại là R
PTHH: \(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(\Rightarrow n_R=0,1\left(mol\right)\) \(\Rightarrow\overline{M}_R=\dfrac{3,26}{0,1}=32,6\)
Ta thấy \(23< 32,6< 39\) \(\Rightarrow\) 2 kim loại cần tìm là Natri và Kali
b) PTHH: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
a_____________a______\(\dfrac{1}{2}\)a (mol)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\uparrow\)
b____________b______\(\dfrac{1}{2}\)b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}23a+39b=3,26\\\dfrac{1}{2}a+\dfrac{1}{2}b=0,05\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,04\\b=0,06\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Na}=\dfrac{0,04\cdot23}{3,26}\cdot100\%\approx28,22\%\\\%m_K=71,78\%\end{matrix}\right.\)
c) PT ion: \(OH^-+H^+\rightarrow H_2O\)
0,1____0,1
Ta có: \(n_{H^+}=n_{HCl}=0,1\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{0,1\cdot36,5}{5\%}=73\left(g\right)\)

Gọi công thức chung của hai kim loại kiềm là \(\overline{M}\)
Có phản ứng:
\(\overline{M}\)\(+H_2O\rightarrow\overline{M}OH+\frac{1}{2}H_2\)
Do đó hỗn hợp cần có 1 kim loại có khối lượng mol nhỏ hơn 31 và 1 kim loại có khối lượng mol lớn hơn 31.
Mà hai kim loại kiềm thuộc hai chu kì liên tiếp
Nên hai kim loại kiềm trong hỗn hợp là Na và K.




Đáp án B
Gọi công thức chung của hai kim loại kiềm là M
Có phản ứng:
Do đó hỗn hợp cần có 1 kim loại có khối lượng mol nhỏ hơn 31 và 1 kim loại có khối lượng mol lớn hơn 31.
Mà hai kim loại kiềm thuộc hai chu kì liên tiếp
Nên hai kim loại kiềm trong hỗn hợp là Na và K.