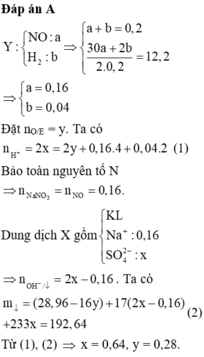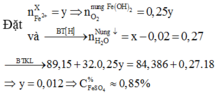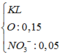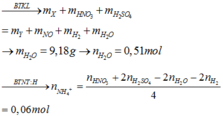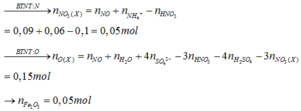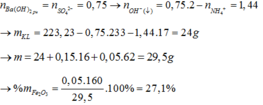Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt khối lượng kim loại trong hỗn hợp ban đầu là m gam; số mol O trong hoonx hợp ban đầu là a mol; số mol H2SO4 là b mol.
![]()
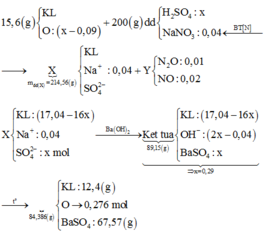
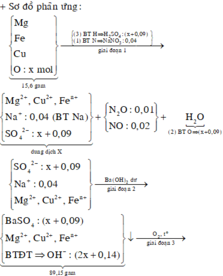
Sơ đồ phản ứng:
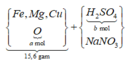
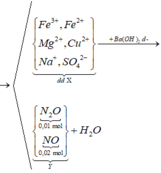
![]()
![]()
Các quá trình tham gia phản ứng của H+: 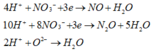
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
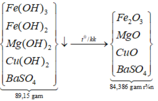
*Xét giai đoạn nung kết tủa đến khối lượng không đổi:
Sơ đồ phản ứng:
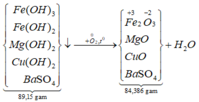
![]()
![]()
![]()
![]()
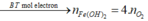
![]()
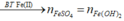
![]()
![]()
![]()
![]() = 85%.
= 85%.
Đáp án A.

Đáp án : A
Ta có : MY = 24,4 => Có H2. Lại có 1 khí hóa nâu ngoài không khí => NO
Áp dụng qui tắc đường chéo ta có : nH2= 0,025 mol ; nNO = 0,1 mol
Do Zn dư và tạo ra khí H2 => NO3 hết => trong dung dịch sau không còn NO3-
Bảo toàn N : nNH4+ = nNO3 ban đầu – nNO = 0,05 mol
=> 2nZn = 2nH2 + 3nNO + 8nNH4+ => 0,375 mol = nZn2+
Bảo toàn điện tích : 2nZn2+ + nNa+ + nK+ + nNH4+ = nCl
=> nCl- = 0,95 mol
=> m = 64,05g