Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C.
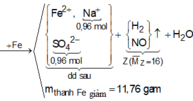
Quy đổi hỗn hợp tương đương với hỗn hợp gồm a mol Fe, b mol OH và c mol O.
Khí Z gồm H2 và NO.
n t h a n h F e p ư = 11 , 76 56 = 0 , 21 m o l
Dung dịch cuối cùng chứa Fe2+, Na+, S O 4 2 -
→ B T N T 2 a + 2 . 0 , 21 + 0 , 96 = 2 . 0 , 96
⇒ a = 0 , 27
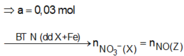
⇒ n H 2 = 0 , 03 m o l n N O = 0 , 03 m o l → B T N T N x = 0 , 13 m o l

Đáp án : A
Dd Y + dd AgNO3:
3Fe2+ + 4H+ + NO3 – → 3 Fe3+ + NO + 2H2O
0,06← 0,08← 0,02 ← 0,02
Kết tủa gồm AgCl và Ag. Trong đó: n AgCl = n HCl = 0,88 mol
=> m Ag = 133,84 – 0,88. 143,5 = 7,56 gam
=> n Ag = 0,07 mol
Fe2+ + Ag+ → Fe3+ + Ag
0,07← 0,07 0,07 0,07
=> ∑ n Fe2+ (ddY) = 0,06 + 0,07 = 0,13 mol
n H+ dư (ddY) = 0,08 mol
=> dd Y gồm Fe+ ; Fe3+; H+ và Cl –
Bảo toàn điện tích trong dd có: 2 n Fe2+ + 3n Fe3+ + n H+ = n Cl –
<=> 3 n Fe3+ = 0,88 – 2. 0,13 – 0,08 = 0,54 mol
<=> n Fe3+ = 0,18 mol
Mặt khác, có ∑ n H+ bđ = 0,88 + 0,04 = 0,92 mol
=> n H+ p.ư = 2. n H2O = 0,84 mol
=> n H2O = 0,42 mol
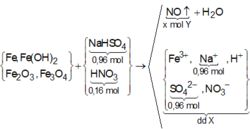
X + HCl + HNO3 → Muối + axit dư + khí + H2O
(0,88 mol) (0,04 mol)
BTKL => m khí = 27,04 + 0,88. 36,5 + 0,04. 63 – 0,42. 18 – 0,31. 56 – 0,08 – 0,88. 35,5 = 5,44 gam
Gọi n N2O = x mol; n NO = y mol
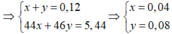
BT nguyên tố N: có n N [Fe(NO3)2] + n N(HNO3) = n N(sp khử)
=> 2. n Fe(NO3)2 + 0,04 = 0,04. 2 + 0,08 = 0,16
=> n Fe(NO3)2 = 0,06 mol
=> m Fe + m FeO + m Fe2O3 + m Fe3O4 (hhX) = 27,04 – 0,06. 180 = 16,24 gam (I)
Mặt khác, n FeO : Fe3O4 : n Fe2O3 = 3: 2: 1
=> Đặt n Fe2O3 = a => n Fe3O4 = 2a và n FeO = 3a
Đặt n Fe = b
Theo (I) => 56b + 840 a = 16,24 (1)
∑ n Fe(I) = 0,31 – 0,06 = 0,25 <=> b + 11a = 0,25 (2)
Từ (1) và (2) => a = 0,01 và b = 0,14 mol
=> % m Fe = (0,14. 56) : 27,04 = 28,99%

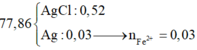
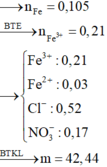




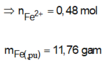
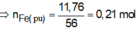
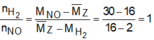
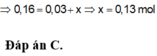
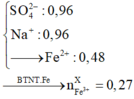
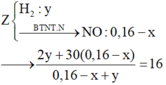

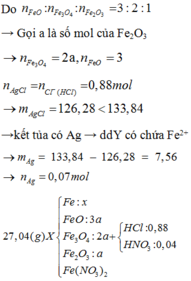
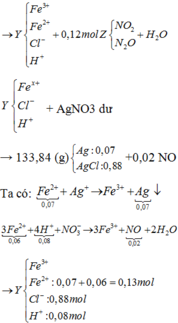

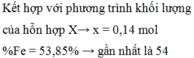

Định hướng tư duy giải
Ta có: nFe = 0,105