
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



CTHH chung của hợp chất là \(Ba_x\left(PO_4\right)_y\left(x,y\in N\text{*}\right)\)
Theo QT hoá trị, ta có: \(x.II=y.III\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{2}\)
Mà \(x,y\in N\text{*}\)
\(\Rightarrow\left\{{}\begin{matrix}x=3\\y=2\end{matrix}\right.\)
Vậy CTHH của hợp chất là \(Ba_3\left(PO_4\right)_2\)
=> Chọn D

Câu 3 :
Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Pt : Fe + H2SO4 → FeSO4 + H2\(|\)
1 1 1 1
0,1 0,1 0,1 0,1
a) Số mol của khí hidro
nH2 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,1 . 22,4
= 2,24 (l)
b) Số mol của muối sắt (II) sunfat
nFeSO4 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Khối lượng của muối sắt (II) sunfat
mFeSO4 = nFeSO4 . MFeSO4
= 0,1 . 152
= 15,2 (g)
c) Số mol của dung dịch axit sunfuric
nH2SO4 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
200ml = 0,2l
Nồng độ mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Chúc bạn học tốt
Câu 4 :
Số mol của photpho
nP = \(\dfrac{m_P}{M_P}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
Pt : 4P + 5O2 → (to) 2P2O5
4 5 2
0,2 0,25 0,1
a) Số mol của đi photpho pentaoxit
nP2O5 = \(\dfrac{0,2.2}{4}=0,1\left(mol\right)\)
Khối lượng của đi photpho pentaoxit
mP2O5 = nP2O5 . MP2O5
= 0,1 . 142
= 14,2 (g)
b) Số mol của khí oxi
nO2 = \(\dfrac{0,2.5}{4}=0,25\left(mol\right)\)
Thể tích của khí oxi ở dktc
VO2 = nO2 . 22,4
= 0,25 . 22,4
= 5,6 (l)
c) Pt : CH4 + 2O2 → CO2 + 2H2O\(|\)
1 2 1 2
0,25 0,125
Số mol của khí cacbonic
nCO2 = \(\dfrac{0,25.1}{2}=0,125\left(mol\right)\)
Thể tích của khí cacbonic ở dktc
VCO2 = nCO2 . 22,4
= 0,125 . 22,4
= 2,8 (l)
Chúc bạn học tốt

Bài 3 :
a) $Zn + 2HCl \to ZnCl_2 + H_2$
b) $n_{H_2} = n_{Zn} = \dfrac{6,5}{65} = 0,1(mol)$
$V_{H_2} = 0,1.22,4 = 2,24(lít)$
c) $n_{ZnCl_2} = n_{Zn} = 0,1(mol)$
$m_{ZnCl_2} = 136.0,1 = 13,6(gam)$
Bài 4 :
a) $2Zn + O_2 \xrightarrow{t^o} 2ZnO$
b)
$n_{Zn} = \dfrac{6,5}{65} = 0,1(mol)$
$n_{O_2} = \dfrac{1}{2}n_{Zn} = 0,05(mol)$
$V_{O_2} = 0,05.22,4 = 1,12(lít)$
c) $n_{ZnO} = n_{Zn} = 0,1(mol) \Rightarrow m_{ZnO} = 0,1.81 = 8,1(gam)$

1.
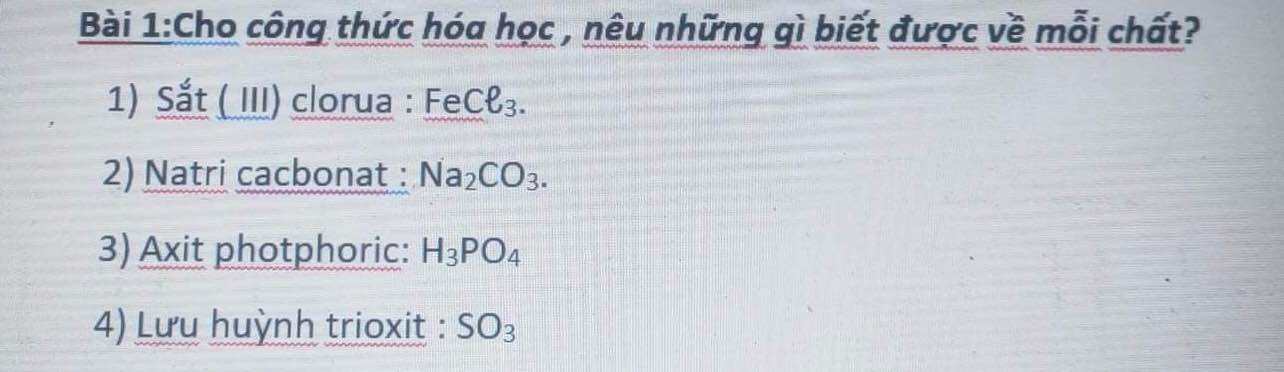
- Hợp chất cấu tạo từ 2 nguyên tố: Fe và Cl
- Hợp chất có: 1 nguyên tố Fe và 3 nguyên tố Cl
- \(PTK=56+35,5\text{ x }3=162,5\left(đvC\right)\)
===========
2.
- Hợp chất cấu tạo từ 3 nguyên tố: Na, C và O
- Hợp chất có: 2 nguyên tố Na, 1 nguyên tố C và 3 nguyên tố O
- \(PTK=23\text{ x }2+12+16\text{ x }3=106\left(đvC\right)\)
==========
3.
- Hợp chất cấu tạo từ 3 nguyên tố: H, P và O
- Hợp chất có: 2 nguyên tố H, 1 nguyên tố P và 4 nguyên tố O
- \(PTK=1\text{ x }3+31+16\text{ x }4=98\left(đvC\right)\)
==========
4.
- Hợp chất cấu tạo từ 2 nguyên tố: S và O
- Hợp chất có: 1 nguyên tố S và 3 nguyên tố O
- \(PTK=32+16\text{ x }3=80\left(đvC\right)\)


\(n_{O_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
a)
PTHH: C + O2 --to--> CO2
1,5<-1,5----->1,5
=> mC = 1,5.12 = 18 (g)
VCO2 = 1,5.22,4 = 33,6 (l)
b)
PTHH: S + O2 --to--> SO2
1,5<-1,5------->1,5
=> mS = 1,5.32 = 48 (g)
VSO2 = 1,5.22,4 = 33,6 (l)
c)
PTHH: 4P + 5O2 --to--> 2P2O5
1,2 <-1,5------->0,6
=> mP = 1,2.31 = 37,2 (g)
mP2O5 = 0,6.142 = 85,2 (g)


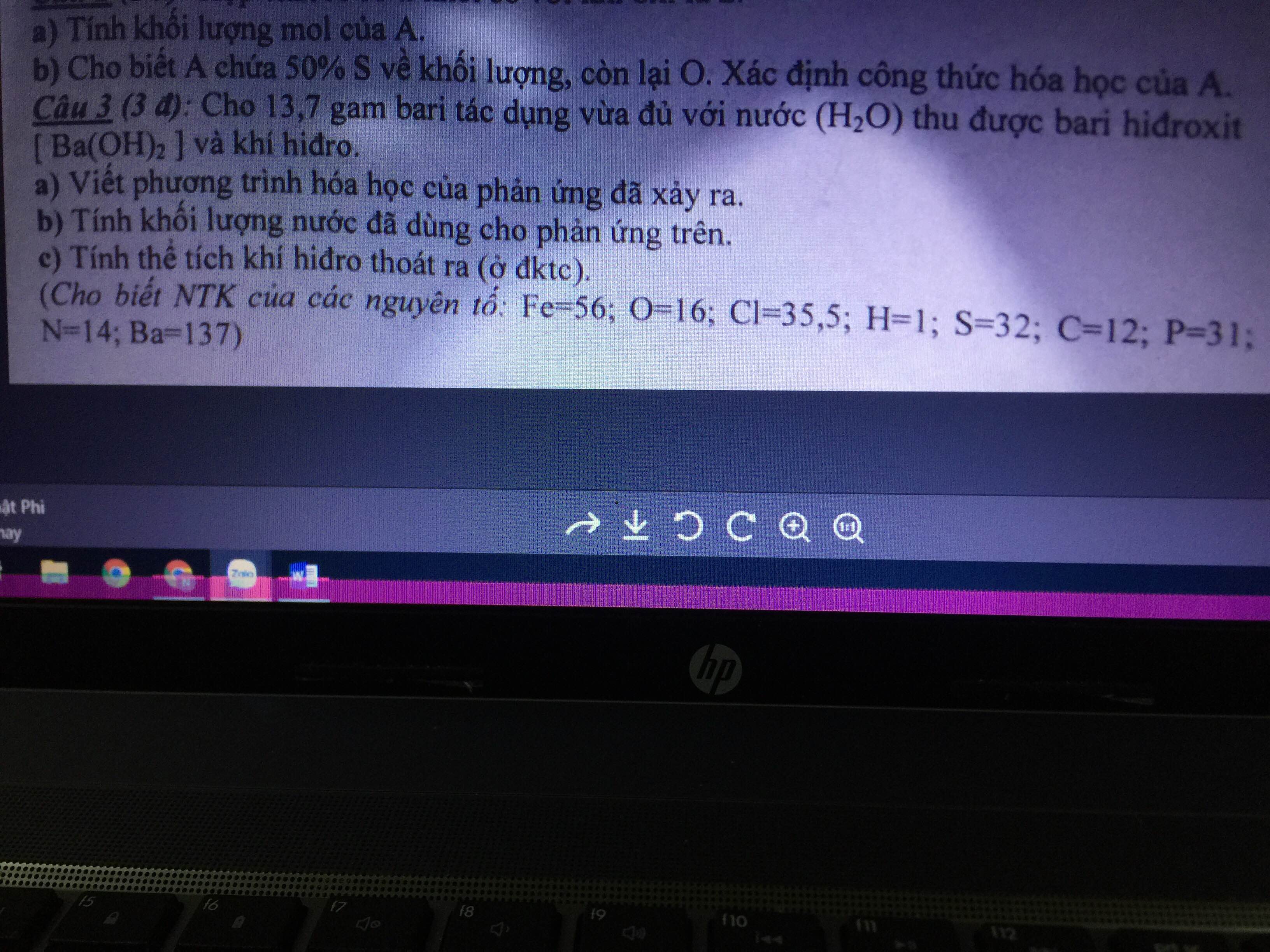





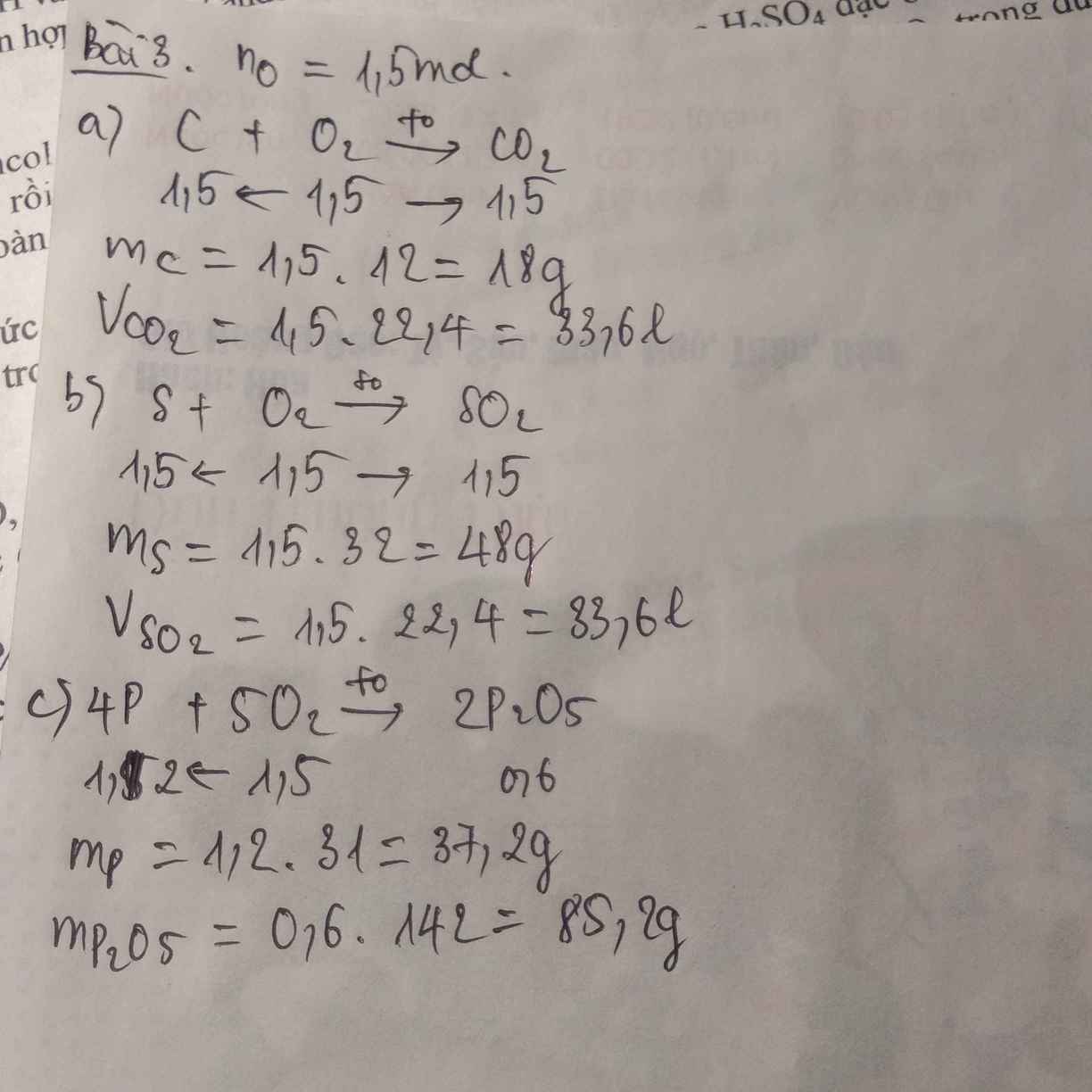


\(a.PTHH:Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(b.n_{Ba}=\dfrac{m}{M}=\dfrac{13,7}{137}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2O}=\dfrac{1}{2}.n_{Ba}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\\ \Rightarrow m_{H_2O}=n.M=0,9\left(g\right)\)
\(c.n_{Ba}=0,1\left(mol\right)\Rightarrow n_{H_2}=n_{Ba}=0,1\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=n.22,4=0,1.22,4=2,24\left(l\right)\)