K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Dưới đây là một vài câu hỏi có thể liên quan tới câu hỏi mà bạn gửi lên. Có thể trong đó có câu trả lời mà bạn cần!

1 tháng 1 2019
Đáp án C
So với TN1, TN2 có nồng độ chất B giảm 2 lần, nồng độ chất A giữ nguyên, làm cho tốc độ phản ứng giảm 2 lần. Kết luận tốc độ phản ứng tỉ lệ thuận với nồng độ chất B.
So với TN1, TN3 có nồng độ chất A tăng 4 lần, nồng độ chất B giữ nguyên, làm cho tốc độ phản ứng tăng 16 lần. Kết luận tốc độ phản ứng tỉ lệ thuận với bình phương nồng độ chất A

30 tháng 3 2017
(a) v tăng lên 83 lần
(b) v tăng lên 23 = 8 lần
(c) v tăng lên 4.22 = 16 lần
(d) v tăng lên 42/2 = 8 lần
Đáp án B

2 tháng 3 2019
Đáp án C
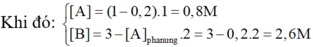
Tốc độ phản ứng lúc đó:
v = k[A].[B]2=0,5.0,8.[2,6]2 =2,704 (mol/l.s)

13 tháng 2 2019
Đáp án C
Khi đó:
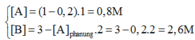
Tốc độ phản ứng lúc đó:
v = k[A].[B]2=0,5.0,8.[2,6]2 =2,704 (mol/l.s)

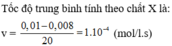

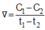
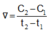
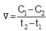
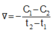

a) v = k . CX.CY
Trong đó k là hằng số tốc độ phản ứng
CX.CY lần lượt là nồng độ của X và Y tại một thời điểm đang xét
b)
- Tốc độ phản ứng tại thời điểm đầu:
v = k . CX.CY = 2,5 . 10-4 . 0,02 . 0,03 = 1,5 . 10-7(mol/(Ls))
- Tốc độ phản ứng tại thời điểm hết một nửa lượng X
=> CX= 0,01 M
CY = 0,02 M
v = k . CX.CY = 2,5 . 10-4 . 0,01 . 0,02 = 5.10-8(mol/(Ls))