Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nCO2 (2)>nCO2 (1) nên ở thí nghiệm (1) H+ hết
*TN1: y < V-x <2y
H+ + OH- → H2O
x x
H+ + CO32- → HCO3-
y y y
H+ + HCO3- → CO2 + H2O
x ← x
=> nH+ = nHCl => 2x + y = V (1)
*TN2: H+ hết
H+ + OH- → H2O
x x
2H+ +CO32- → CO2 + H2O
3,2x ← 1,6x
=> => nH+ = nHCl => 4,2x = V (2)
(1) và (2) => 2x + y = 4,2x => 2,2x = y => x : y = 1:2,2 = 5 : 11

Đáp án B
► Xét TN1: đặt nCO32– phản ứng = a; nHCO3– phản ứng = b.
⇒ nCO2 = a + b = 0,15 mol; nHCl phản ứng = 2a + b = 0,1875 mol
||⇒ giải hệ có: a = 0,0375 mol; b = 0,1125 mol ⇒ nCO32–/X : nHCO3–/X = a : b = 1 : 3.
► Xét TN2: ∑nC/X = n↓ = 0,25 mol ⇒ 250 ml X chứa 0,5 mol C.
Bảo toàn nguyên tố Cacbon: y = 0,5 – 0,25 = 0,25 mol.
● Chia 0,5 mol C thành 0,125 mol CO32– và 0,375 mol HCO3–.
Bảo toàn điện tích: nK+ = 0,625 mol. Bảo toàn nguyên tố Kali:
x = 0,625 – 0,25 × 2 = 0,125 mol

Đáp án B
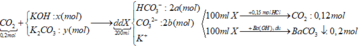
TH1: Nếu trong dd X có OH- dư => dd X chứa OH- dư, CO32-, K+
Khi cho từ từ 100 ml dd X vào 0,15 mol HCl
OH- + H+ → H2O
CO32- + 2H+ → CO2 ↑+ H2O
=> nH+ = nOH- + 2nCO2 > 0,12.2 = 0,24 (mol)
=> loại vì nH+ = 0,15 (mol)
Vậy dd X không chứa OH- dư
TH2: dd X không chứa OH- dư ta có sơ đồ bài toán như trên
Khi cho từ từ 100ml dd X vào 0,15 mol HCl có phản ứng:
HCO3- + H+ → CO2 + H2O
x → x →x (mol)
CO32- + 2H+ → CO2 + H2O
y → 2y → y (mol)

=> a – 3b = 0 (1)
BTNT C: nBaCO3 = a + b = 0,2 (2)
Từ (1) và (2) => a = 0,15 và b = 0,05 (mol)
Trong 200 ml dd X : nHCO3- = 0,3 (mol) ; nCO32- = 0,1 (mol)
Bảo toàn điện tích đối với dd X : nK+ = 0,3 + 0,1.2 = 0,5 (mol)
BTNT C: nCO2(bđ) + nK2CO3 = nHCO3-+ nCO32- => 0,2 + y = 0,3 + 0,1 => y = 0,2 (mol)
BTNT K: nK+ = nKOH + 2nK2CO3 => nKOH = 0,5 – 2.0,2 = 0,1 (mol)
=> x = 0,1 (mol)

Đáp án D
Có n C O 2 b a n đ ầ u = 0,2; n C O 2 s ả n p h ẩ m p h ầ n 1 = 0,12; n B a C O 3 = 0,2
Dung dịch X thu được chứa K2CO3 và KOH dư hoặc K2CO3 và KHCO3
Khi cho 200 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư thu được 0,4 mol kết tủa. Dù thành phần của X gồm những chất nào thì ta luôn có:
n B a C O 3 = n C O 2 b a n đ ầ u + n K 2 C O 3
= 0,2 + y = 0,4 ⇔ y = 0,2
+) Trường hợp 1: Dung dịch X chứa K2CO3 và KOH dư.
Khi đó ở mỗi phần gọi n K 2 C O 3 = a ; n K O H = b
Bảo toàn nguyên tố C, ta có:
2a = n K 2 C O 3 b a n đ ầ u + n C O 2 b a n đ ầ u = 0,4 ⇔ a = 0,2
Khi cho 100ml dung dịch X từ từ vào 300 ml dung dịch HCl 0,5M (0,15 mol HCl) thì xảy ra các phản ứng sau:
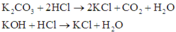
Mà thực tế nHCl < 0,24
Nên trường hợp này không thỏa mãn.
+) Trường hợp 2: Dung dịch X chứa K2CO3 và KHCO3
Khi đó ở mỗi phần gọi n K 2 C O 3 = a ; n K O H = b
Bảo toàn nguyên tố C, ta có:
n B a C O 3 = n K 2 C O 3 + n K H C O 3 = a + b = 0,2 (*)
Khi cho 100ml dung dịch X từ từ vào 300ml dung dịch HCl 0,5M (0,15 mol HCl) thì các phản ứng sau xảy ra đồng thời:
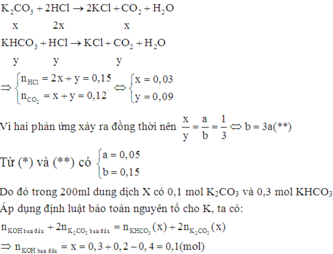

Đáp án B
Ta có: n C O 2 = 0,15 mol; n C O 2 (phần 1)= 0,09 mol ; n B a C O 3 = 0,15 mol
Giả sử xảy ra các phản ứng:
CO2+ NaOH→ Na2CO3+ H2O
CO2+ Na2CO3+H2O → 2 NaHCO3
Dung dịch X chứa z mol NaHCO3 và t mol Na2CO3
Xét phần 1 ta có: giả sử có x mol NaHCO3 và y mol Na2CO3 phản ứng
NaHCO3+ HCl → NaCl + CO2+ H2O
Na2CO3+ 2HCl → 2NaCl + CO2+ H2O
Ta có: nHCl = x+2y = 0,12 mol;
n C O 2 = x+y = 0,09 mol
→x = 0,06 và y = 0,03
→ z t = x y = 0 , 06 0 , 03 = 2 → z = 2 t ( * 1 )
Xét phần 2 :
HCO3- + OH- → CO32-+ H2O
0,5z 0,5z
CO32- + Ba2+ → BaCO3 ↓
(0,5z+0,5t)→ (0,5z+0,5t)
→ n B a C O 3 = 0,5z+ 0,5t = 0,15 (*2)
Từ (*1) và (*2) ta có: z = 0,2 mol; t = 0,1 mol
→Dung dịch X chứa 0,2 mol NaHCO3 và 0,1 mol Na2CO3
Quay lại 2 phản ứng đầu :
CO2+ 2NaOH→ Na2CO3+ H2O (1)
0,05→ 0,1 0,05
CO2+ Na2CO3+H2O → 2 NaHCO3 (2)
0,1 0,1 ← 0,2 mol
Ta có: n C O 2 PT 1 = n C O 2 - n C O 2 PT 2 = 0,15- 0,1 = 0,05 mol
Theo PT (1) : nNaOH = a = 0,1 mol
Số mol Na2CO3 còn sau phản ứng (2) là:
b+ 0,05- 0,1 = 0,1→ b = 0,15
Do đó a b = 0 , 1 0 , 15 = 2 3

Đáp án A
Vì thể tích CO2 thu được ở hai lần thí nghiệm khác nhau nên cả hai trường hợp HCl đều hết, chất phản ứng còn lại dư vì nếu ở cả hai trường hợp có các chất đều phản ứng vừa đủ hoặc HCl dư thì lượng CO2 thu được như nhau (bảo toàn nguyên tố C).
Khi cho từ từ từng giọt dung dịch HCl vào dung dịch Na2CO3 có thứ tự các phản ứng xảy ra như sau:
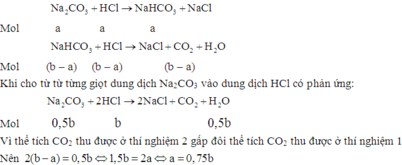

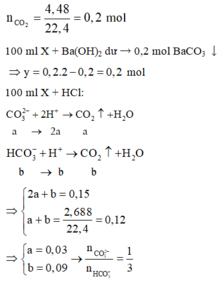
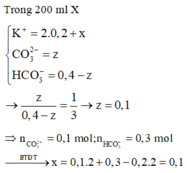



Đáp án B
TN1: nCO2 = 3,36/22,4 = 0,15 (mol);
+ Cho từ từ HCl vào dd Y sẽ xảy ra phản ứng theo thứ tự:
H+ + CO32-→ HCO3-
H+ + HCO3- → CO2 ↑+ H2O
Áp dụng công thức nhanh => nCO2 = nH+ - nCO32-
=> a – c = 0,15 (1)
TN2: nCO2 = 10,08/ 22,4 = 0,45 (mol)
+ Cho từ từ dd Y vào HCl thì xảy ra đồng thời
HCO3- + H+ → CO2 + H2O
2x → 2x → 2x (mol)
CO32- + 2H+ → CO2 + H2O
x →2x → x (mol)
Vì => phản ứng cũng xảy ra theo tỉ lệ mol như này.
Gọi nCO32- = x thì nHCO3 = 2x
=> nCO2 = 3x = 0,45 (mol) => x = 0,15 (mol)
∑nH+ = 4x = 4. 0,15 = 0,6 (mol) = a
Từ (1) => c = 0,45 (mol)
=> a + b + c = 0,15 + 0,9 + 0,45 = 1,5