Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi cho 5g Br 2 có lẫn Cl 2 phản ứng với KBr thì khối lượng muối giảm là :
1,600 - 1,155 = 0,445 (g)
Cl 2 + 2KBr → 2KCl + Br 2
Lý thuyết: 71 g 238 g 149 g khối lượng muối giảm đi 238 – 149 = 89 g
Thực tế: x g 0,445 g khối lượng muối giảm
Ta có:
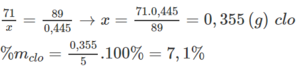

Có lẽ đề cho nung kết tủa trong không khí chứ không phải "để" bạn nhỉ?
PT: \(Zn+CuSO_4\rightarrow ZnSO_4+Cu\)
____0,04_____0,04_____0,04 (mol)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
0,03_____0,03______0,03 (mol)
⇒ nCuSO4 dư = 0,1 - 0,04 - 0,03 = 0,03 (mol)
- Dung dịch X gồm: ZnSO4: 0,04 (mol), FeSO4: 0,03 (mol) và CuSO4: 0,03 (mol)
PT: \(ZnSO_4+Ba\left(OH\right)_2\rightarrow Zn\left(OH\right)_{2\downarrow}+BaSO_{4\downarrow}\)
______0,04__________________0,04______0,04 (mol)
\(Zn\left(OH\right)_2+Ba\left(OH\right)_2\rightarrow BaZnO_2+2H_2O\)
\(FeSO_4+Ba\left(OH\right)_2\rightarrow Fe\left(OH\right)_{2\downarrow}+BaSO_{4\downarrow}\)
0,03____________________0,03______0,03 (mol)
\(CuSO_4+Ba\left(OH\right)_2\rightarrow Cu\left(OH\right)_{2\downarrow}+BaSO_{4\downarrow}\)
0,03____________________0,03_______0,03 (mol)
- Kết tủa thu được gồm: Fe(OH)2: 0,03 (mol), Cu(OH)2: 0,03 (mol) và BaSO4: 0,1 (mol)
PT: \(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
_________0,03_________0,015 (mol)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
0,03_________0,03 (mol)
⇒ m = mFe2O3 + mCuO + mBaSO4 = 0,015.160 + 0,03.80 + 0,1.233 = 28,1 (g)

Câu 1 :
\(N_{Anken}=\frac{11,2}{22,4}=0,05\left(mol\right)\)
\(n_{H2O}=\frac{3,6}{18}=0,2\left(mol\right)\)
Do là 1 anken nên \(n_{CO2}=n_{H2O}=0,2\left(mol\right)\)
Số C trong anken là: \(\frac{n_C}{n_{Anken}}=\frac{0,2}{0,05}=4\)
Vậy CTPT là C4H8
Câu 2 :
\(_{Br2}=0,1\left(mol\right)\)
\(n_{Br2}=n_{Anken}=0,1\left(mol\right)\)
\(PTHH:C_2H_{2n}+Br_2\rightarrow C_nH_{2n}Br_2\)
\(M=\frac{4,2}{0,1}=42\)
Công thức chung của anken là CnH2n=14n
\(\Leftrightarrow14n=42\Leftrightarrow n=3\)
Vậy CTPT của X là C3H6
Câu 3:
\(CH_2=CH-CH=CH_2+Br_2\underrightarrow{^{80^o}}CH_2Br-CHBr-CH=CH_2\)
\(CH_2=CH-CH=CH_2+Br_2\underrightarrow{^{40^o}}CH_2Br-CH=CH-CH_2Br\)
\(nCH_2=C\left(CH_3\right)-CH=CH_2\rightarrow\left(-CH_2-C\left(CH_3\right)=CH-CH_2-\right)n\)

Có 4 đồng phân amin thỏa mãn điều kiện đề bài 2 amin bậc I, 1 amin bậc II và 1 amin bậc III
Đáp án C

a)\(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}64x+27y=9,1\\BTe:2x+3y=0,5\cdot1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{0,1\cdot64}{9,1}\cdot100\%=70,33\%\)
\(\%m_{Al}=100-70,33\%=29,67\%\)
b)\(\left\{{}\begin{matrix}n_{NO_2}+n_{NO}=0,5\\\dfrac{n_{NO_2}}{n_{NO}}=\dfrac{2}{1}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{NO_2}=\dfrac{1}{3}\\n_{NO}=\dfrac{1}{6}\end{matrix}\right.\)
Gọi \(\left\{{}\begin{matrix}n_{Cu}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}64a+27b=9,1\\BTe:2x+3y=\dfrac{1}{3}\cdot1+\dfrac{1}{6}\cdot3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=\dfrac{4}{115}\\b=\dfrac{527}{2070}\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{\dfrac{4}{115}\cdot64}{9,1}\cdot100\%=24,46\%\)
\(\%m_{Al}=100\%-24,46\%=75,54\%\)
\(n_{HNO_3}=2n_{NO_2}+4n_{NO}=2\cdot\dfrac{1}{3}+4\cdot\dfrac{1}{6}=\dfrac{4}{3}mol\)












X có dạng CnH2n
\(C_nH_{2n}+Br_2\rightarrow C_nH_{2n}Br_2\)
\(\Rightarrow\%m_{Br.trong.Y}=\frac{80.2}{14n+80.2}=74,08\%\)
\(\Rightarrow n=4\)
Vậy X là C4H8
X td với Br2 trong dd nên đây là phản ứng cộng
->%Br=160\(MX+160)=74,8%
->MX=56 : C4H8
XcộngHBrthu đc 2 sản phẩm->Xlà but-1-ten