Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
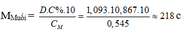
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
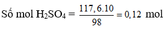
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%

\(M + 2HCl \to MCl_2 + H_2\\ n_M = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ \Rightarrow M = \dfrac{5,6}{0,1} = 56(Fe)\\ \)
Vậy M là kim loại Fe
\(n_{FeCl_2} = n_{H_2} = 0,1(mol)\\ m_{FeCl_2} = 0,1.127 = 12,7(gam)\\ m_{dd\ sau\ pư} =m_{Fe} + m_{dd\ HCl} -m_{H_2} = 5,6 + 94,6 -0,1.2 = 100(gam)\\ C\%_{FeCl_2} = \dfrac{12,7}{100}.100\% = 12,7\%\)

Gọi M là kí hiệu nguyên tử khối của kim loại hoá trị I. Công thức muối là M 2 CO 3 . Phương trình hoá học của phản ứng :
M 2 CO 3 + 2HCl → 2 MCl 2 + H 2 O + CO 2
(2M + 60)g 22400ml
1,06g 224ml
Theo phương trình hóa học trên ta có:
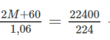
→ M = 23. Đó là muối Na 2 CO 3

M + 2HCl → MCl2 + H2↑
MO + 2HCl → MCl2 + H2O
MCl2 + 2NaOH → M(OH)2↓ + 2NaCl
M(OH)2 → MO + H2O
M + CuCl2 → MCl2 + Cu↓

a)
$MCO_3 \xrightarrow{t^o} MO + CO_2$
$CO_2 + Ba(OH)_2 \to BaCO_3 + H_2O$
$CO_2 + Ba(OH)_2 \to Ba(HCO_3)_2$
b)
$n_{Ba(OH)_2} = 0,15(mol) ; n_{BaCO_3} = \dfrac{19,7}{197} = 0,1(mol)$
$n_{Ba(HCO_3)_2} = n_{Ba(OH)_2} - n_{BaCO_3} = 0,05(mol)$
$n_{CO_2} = n_{BaCO_3} + 2n_{Ba(HCO_3)_2} = 0,2(mol)$
$n_{MCO_3} = n_{CO_2} = 0,2(mol)$
$m_A = m_{MCO_3} - m_{CO_2} = 20 - 0,2.44 = 11,2(gam)$
c)
$M_{MCO_3} = M + 60 = \dfrac{20}{0,2} = 100$
$\Rightarrow M = 40(Canxi)$
Vậy CTHH : $CaCO_3$

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
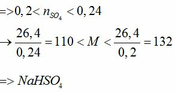
b)
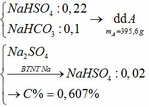
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O

Gọi CTHH của muối là RCO3
nCO2 = \(\frac{3,36}{22,4}\) = 0,15 (mol)
RCO3 + HCl \(\rightarrow\) RCl2 + H2O + CO2
0,15 <------------------------------- 0,15 (mol)
Áp dụng ĐLBTKL ta có:
m + 100 = 110,8 + 0,15 . 44
\(\Rightarrow\) m = 17,4 (g)
Mmuối = \(\frac{17,4}{0,15}\) = 116 (g/mol)
\(\Rightarrow\) R + 60 = 116
\(\Rightarrow\) R = 56 (g/mol)
\(\Rightarrow\) R = 56 đvC (Fe: sắt)
CTHH của muối là FeCO3




\(a)X_2CO_3+2HCl\rightarrow2XCl+CO_2+H_2O\\ \\ b)n_{X_2CO_3}=\dfrac{10,6}{2X+60}mol\\ n_{CO_2}=\dfrac{2,24}{22,4}=0,1mol\\ \Rightarrow n_{CO_2}=n_{X_2CO_3}\\ \Leftrightarrow\dfrac{10,6}{2X+60}=0,1\\ \Leftrightarrow X=23,Na\\ \Rightarrow CTHH:Na_2CO_3\)