Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khối lượng dung dịch H 2 SO 4 50% thu được :
100 tấn dung dịch có 50 tấn H 2 SO 4
x tấn ← 73,5 tấn
x = 73,5x100/50 = 147 tấn

Câu 15 :
\(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,4----->1,2------->0,4------>0,6
\(m_{HCl}=1,2.36,5=43,8\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{43.8.100\%}{25\%}=175,2\left(g\right)\)
\(m_{ddspu}=10,8+175,2-0,6.2=184,8\left(g\right)\)
\(C\%_{AlCl3}=\dfrac{0,4.133,5}{184,8}.100\%=28,9\%\)

nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
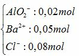 + V ml HCl 1M→ Al(OH)3: 0,01 (mol)
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)

\(a,PTHH:CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ n_{CuSO_4}=n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\\ \Rightarrow m_{CuSO_4}=0,1\cdot160=16\left(g\right)\\ b,n_{H_2SO_4}=n_{CuO}=0,1\left(mol\right)\\ \Rightarrow m_{CT_{H_2SO_4}}=0,1\cdot98=9,8\left(g\right)\\ \Rightarrow C\%_{H_2SO_4}=\dfrac{9,8}{200}\cdot100\%=4,9\%\)

a) \(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
PTHH: CuO + 2HCl --> CuCl2 + H2O
0,05---->0,1----->0,05--->0,05
=> \(C\%\left(HCl\right)=\dfrac{0,1.36,5}{150}.100\%=2,433\%\)
b) \(C\%\left(CuCl_2\right)=\dfrac{0,05.135}{4+150}.100\%=4,383\%\)

\(n_{HCl}=\dfrac{44,8}{22,4}=2\)
\(\Rightarrow m_{HCl}=2.36,5=73g\)
=> \(C\%_{HCl}=\dfrac{73}{73+327}\times100\%=18,25\%\)
b.
\(n_{HCl}=\dfrac{250.18,25\%}{36,5}=1,25mol\)
\(n_{CaCO_3}=\dfrac{50}{100}=0,5mol\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(n_{CaCl_2}=n_{CO_2}=0,5mol\)
\(n_{HClpu}=0,5.2=1mol\)
\(\Rightarrow n_{HCldu}=1,25-1=0,25\)
\(\Rightarrow m_{ddpu}=50+250-0,5.44=278g\)
\(C\%_{HCl}=\dfrac{0,25.36,5}{278}.100\%=3,28\%\)
\(C\%_{CaCl_2}=\dfrac{0,5.111}{278}.100\%=19,96\%\)