Câu 92. Hai nguyên tố X và Y đứng kê tiếp nhau ở cùng một chu kỳ trong bảng tần hoàn (bán kính nguyên tỉ X lớn hơn bán kính nguyên tử Y), có tông số hạt mang điện là 58. a/ Viết cáấu hình electron của nguyên tử X, Y. b/ Xác định vị trí của X, Y trong bảng tuân hoàn và gọi tên nguyên tổ X, Y.
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

5 tháng 8 2018
B
X và Y là hai kim loại cùng nhóm A.
=> Y có nhiều hơn X là 8 hoặc 18 hoặc 32 electron.
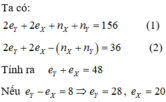
(không thuộc 2 chu kì)(loại).
![]()
Vậy 2 nguyên tố này là As và P, cùng thuộc nhóm VA và thuộc 2 chu kì (nhận).
![]()
(không thuộc 2 chu kì liên tiếp) (loại).
Vậy X là photpho (P).

17 tháng 8 2017
Đáp án D
Hai nguyên tố thuộc cùng một nhóm A, thuộc hai chu kỳ liên tiếp = Điện tích hạt nhân cách nhau 8, 18 hay 32
Trường hợp 1:
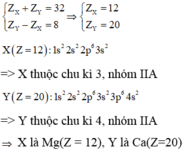
Trường hợp 2:
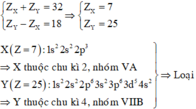
Trường hợp 3:
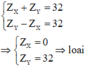

7 tháng 2 2019
Đáp án C
Vì X và Y thuộc cùng một nhóm A và ở chu kì liên tiếp nên ta có:
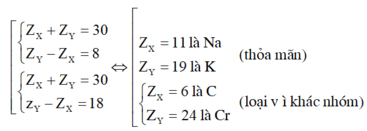
Khi đó cấu hình electron là của Na là 1s22s22p63s1




a) Trong cùng 1 chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử của nguyên tố giảm dần \(\Rightarrow Z_X< X_Y\).
-Vì 2 nguyên tố X,Y đứng kế nhau trong bảng tuần hoàn nên \(Z_X+1=Z_Y\left(1\right)\)
-Vì 2 nguyên tố X,Y có tổng số hạt mang điện là 58 nên \(2\left(Z_X+Z_Y\right)=58\left(2\right)\)
Từ (1), (2) ta có: \(\left\{{}\begin{matrix}Z_X=14\\Z_Y=15\end{matrix}\right.\)
Cấu hình electron của nguyên tử X,Y:
\(X:1s^22s^22p^63s^23p^2\) ; \(Y:1s^22s^22p^63s^23p^3\)
b) Vị trí của X,Y trong bảng tuần hoàn:
X: ô 14, nhóm IVA, chu kì 3. X là Si.
Y: ô 15, nhóm VA, chu kì 3. Y là P.