Trong phòng thí nghiệm người ta dùng hiđro để khử sắt (III) oxi và thu được 12,6 g sắt.
a. Tính khối lượng sắt (III) oxit đã phản ứng;
b. Tính thể tích khí hiđro đã tiêu thụ (ở đktc).
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{11,2}{56}=0,2\) (mol)
Pt : Fe2O3 + 3H2 \(\rightarrow\) 2Fe + 3H2O\(|\)
1 2 2 2
0,1 0,2
Số mol của sắt (III) oxit
nFe2O3 = \(\dfrac{0,2.1}{2}=0,1\) (mol)
Khối lượng của sắt (III) oxit
mFe2O3 = nFe2O3 . MFe2O3
= 0,1 . 160
= 16 (g)
Chúc bạn học tốt
Bạn sửa lại số ghi dưới phương trình của cân bằng khí hidro và nước giúp mình

a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,1\left(mol\right)\Rightarrow m_{Fe_2O_3}=0,1.160=16\left(g\right)\)
c, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)

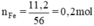
Phương trình hóa học của phản ứng:
Fe2O3 + 3H2 → 2Fe + 3H2O.
Khử 1 mol Fe2O3 cho 2 mol Fe.
x mol Fe2O3 → 0,2 mol.
x = 0,2 : 2 =0,1 mol.
m = 0,1 .160 =16g.
Khử 1 mol Fe2O3 cần 3 mol H2.
Vậy khử 0,1 mol Fe2O3 cần 0,3 mol H2.
V= 0,3 .22.4 = 6,72l.

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(PTHH:Fe_2O_3+3H_2\xrightarrow[]{}2Fe+3H_2O\)
tỉ lệ :1 3 2 3
số mol :0,1 0,3 0,2 0,3
\(m_{Fe_2O_3}=0,1.160=16\left(g\right)\)

2)
nH2 = 6.72/22.4 = 0.3 (mol)
Fe2O3 + 3H2 -to-> 2Fe + 3H2O
0.1______0.3______0.2
mFe2O3 = 0.1*160 = 16 (g)
mFe = 0.2*56 = 11.2 (g)
3)
nFe3O4 = 11.6/232 = 0.05 (mol)
3Fe + 2O2 -to-> Fe3O4
0.15___0.1______0.05
mFe = 0.15*56 = 8.4 (g)
VO2 = 0.1*22.4 = 2.24 (l)
2KClO3 -to-> 2KCl + 3O2
1/15______________0.1
mKClO3 = 1/15 * 122.5 = 8.167 (g)
a)
3H2 + Fe2O3 --to--> 2Fe + 3H2O
b) nH2 = 6,72/22,4 = 0,3 mol
Từ pt => nFe3O4 = 0,1 mol
=> mFe3O4 = 0,1. 232 = 23,2 g

a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe}=\dfrac{24}{56}=\dfrac{3}{7}\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=\dfrac{3}{14}\left(mol\right)\Rightarrow m_{Fe_2O_3}=\dfrac{3}{14}.160=\dfrac{240}{7}\left(g\right)\)
c, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Fe}=\dfrac{9}{14}\left(mol\right)\Rightarrow V_{H_2}=\dfrac{9}{14}.22,4=14,4\left(l\right)\)
\(n_{Fe}=\dfrac{m}{M}=\dfrac{24}{56}\approx0,43\left(mol\right)\\ a.PTHH:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
2 3 2 3
0,43 0,645 0,45 0,645
\(b.m_{Fe_2O_3}=n.M=0,43.\left(56.2+16.3\right)=68,8\left(g\right)\\ c.V_{H_2}=n.24,79=0,645.24,79=15,98955\left(l\right).\)
Fe2O3+3H2-to>2Fe+3H2O
0,1125---0,3375----0,225 mol
n Fe=0,225 mol
=>m Fe2O3=0,1125.160=18g
=>VH2=0,3375.22,4=7,56l