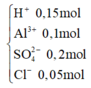
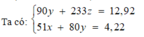Dung dịch X được tạo ra từ 2 muối gồm có các ion Al3+, Fe2+, Cl-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 đem tác dụng với dung dịch Ba(OH)2 dư thu được 6,46 gam kết tủa. Phần 2 đem tác dung với dung dich NH3 dư thu lấy kết tủa nung trong không khí đến khối lượng không đổi còn lại 2,11 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Khối lượng muối trong X có thể là:
A. 3,475 gam
B. 5,96 gam
C. 8,75 gam
D. 17,5 gam