Hoà tan hoàn toàn m gam bột Al vào 140 ml dung dịch HCl 2M thu được dung dịch X. Cho dung dịch X tác dụng với 340 ml dung dịch NaOH 1M thu được 0,78 gam kết tủa. Giá trị của m là:
A. 2,16 gam
B. 1,62 gam
C. 2,7 gam
D. 1,89 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án : D
, nHCl = 0,3 mol ; nNaOH = 0,32 mol ; nAl(OH)3 = 0,06 mol
Vì nNaOH > nHCl => dư OH sau khi phản ứng hết với AlCl3 => có hiện tượng hòa tan kết tủa
=> nOH tan kết tủa = nNaOH – nHCl = 0,02 mol
=> nAl(OH)3 max = 0,06 + 0,02 = 0,08 mol = nAl bđ
=> mAl = 2,16g

Đáp án A
Từ giả thiết suy ra : Ở TN2 đã có hiện tượng hòa tan kết tủa. Còn ở TN1 thì có thể có hiện tượng hòa tan kết tủa hoặc chưa. Ta đặt :
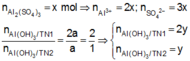
● Nếu cả TN1 và TN2 đều có hiện tượng hòa tan kết tủa, áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
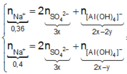
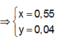
![]() thỏa mãn
thỏa mãn
Suy ra : ![]()
● Nếu TN1 chưa có hiện tượng hòa tan kết tủa, áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
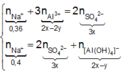
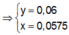
![]() (loại)
(loại)

Đáp án : C
Giả sử cả 2 trường hợp đều có hiện tượng hòa tan kết tủa
Xét công thức tính nhanh chung : nOH = 4nZn2+ - 2nZn(OH)2
+) TN1 : 0,22 = 4nZn2+ - 2.3a/99
+) TN2 : 0,28 = 4nZn2+ - 2.2a/99
=> nZn2+ = 0,1 mol => m = 16,1g

Đáp án D
nAl = 0,02 mol; nCl– = 0,07 mol; nNa+ = 0,075 mol.
Ghép NaCl
⇒ còn dư (0,075 – 0,07 = 0,005) mol Na+
⇒ ghép với AlO2– tạo NaAlO2.
||⇒ ghép được 0,005 mol NaAlO2 và còn dư (0,02 – 0,005 = 0,015) mol nguyên tố Al.
► Dùng nguyên tố đó ghép vào ↓ ⇒ nAl(OH)3 = 0,015 mol
⇒ m = 1,17(g)