Tính pH của dung dịch hỗn hợp CH3COOH 0,1M và CH3COONa 0,1M. Biết rằng ở một nhiệt độ xác định t°C có K a C H 3 C O O H = 1 , 8 . 10 - 5
A. 1
B. 1,745
C. 1,754
D. 1,7
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sửa đề bài Vì CH3COONa là chất điện li mạnh nên được viết trước để tạo môi trường cho cân bằng của chất điện li yếu phân li và cân bằng:
CH³COOH ⇔ CH³COO -+H+
Ban đầu 0,1 0. 0
Phân li xM x. x
Cân bằng 0,1-x 0,1+x x
Suy ra K = \(\dfrac{x(x+0,1)}{0,1-x}\) = 1,8.10 mũ âm ⁵
⇒ x = 1,8 . 10 mũ âm ⁵
⇒pH = log x = 1745

Vì muối CH3COONa là chất điện li mạnh nên ta có
![]()
Do đó sau quá trình trên trong dung dịch có nồng độ của ion CH3COO- là 0,1.
Xét cân bằng điện li: CH3COOH + H2O ⇌ CH3COO- + H3O+
Nồng độ ban đầu: 0,1 0,1 0
Nồng độ phân li: x(M) → x x
Nồng độ cân bằng: 0,1 – x 0,1 + x x
Thay các giá trị ở trạng thái cân bằng vào công thức tính hằng số điện li thì ta có
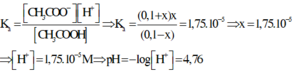
Đáp án D.

dung dịch Z có pH=13-> dung dịch Z chứa OH có nồng độ là 0,1M
ta có \(n_{H^+}=0,5a\) mol ,\(n_{OH}\) = 0,5b mol
\(H^++OH\rightarrow H_2O\)
dung dịch Z chứa OH \(\rightarrow n_{OHdư}=0,5b-0,5a\) mol
\(\rightarrow\left[OH-\right]=\frac{0,5b-0,5a}{a+b}=0,1M\rightarrow0,4b-0,6a=0\left(1\right)\)
theo đề bài -> a + b = 1 (2)
giải hệ chứa (1) và (2) -> a = 0,4 và b = 0,6

Gọi \(\left\{{}\begin{matrix}n_{O2}:a\left(mol\right)\\n_{O3}:b\left(mol\right)\end{matrix}\right.\)
\(PTHH:O_3+2KI+H_2O\rightarrow O_2+I_2+2KOH\)
\(\overline{M_A}=10,24.4=40,96\)
Sau khi dẫn qua KI , \(\Rightarrow V_{O2}=\frac{50}{22,4}\left(mol\right)\)
Giải hệ PT:
\(\left\{{}\begin{matrix}a+b=\frac{50}{22,4}\\\frac{32a+48b}{a+b}=40,96\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=\frac{55}{56}\\b=1,25\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{O2}=\frac{55}{56}.22,4=22\left(l\right)\\V_{O3}=1,25.22,4=28\left(l\right)\end{matrix}\right.\)
Gọi a là số mol của O3 thêm
\(\overline{M}=10,667.4=42,668\)
\(\Rightarrow\frac{\frac{55}{56}.32+48\left(1,25+a\right)}{\frac{50}{22,4}+a}=42,668\)
\(\Leftrightarrow48\left(1,25+a\right)+\frac{220}{7}=42,668\left(\frac{50}{22,4}+a\right)\)
\(\Leftrightarrow a=0,715\)
\(\Rightarrow V_{O3}=0,715.22,6=16,0,16\left(l\right)\)
Bạn xem lại ý c nhé!

a)CH3COONa->CH3COO(-)+Na(+)
.........................Bazo....trung tinh
.....0,1M..................0,1M
...CH3COO(-)+H2O---->CH3COOH+OH(-)
bd 0,1M
pu...x................................x...
cb...0,1-x...........................x....
Kb=x^2/(0,1-x)=5,71x10^(-10)
=>x^2+5,71x10^(-10) - 5,71x10^(-11)=0
=>x=7,6x10^(-6)
=>[H(+)]=x
b)NH4Cl------>NH4(+)+Cl(-)
.....................axit.....trung tinh
....0,1M...........0,1M
....NH4(+)+H2O--->NH3+H3O
bd..0,1M
pu..x.......................x......x
cb..0,1-x.................x.......x
Ka=x^2/(0,1-x)=5,56x10^(-10)
=>x^2+5,56x10^(-10) - 5,56x10^(-11)=0
=>x=7,5x10^(-6)
=>[H3O]=x
a) CH3COONa → CH3COO- + Na+
0,2 0,2
CH3COOH ↔ CH3COO- + H+
Ban đầu: 0,1 0,2 0
Phân ly: x x x
Cân bằng: 0,1-x 0,2+x x
KaCH3COOH=(0,2+x).x/(0,1-x)= 1,8.10-5
→x= nồng độ cân bằng của H+= 9.10-5
b) câu này chưa có KaNH4 → thiếu đề

bạn thử làm như sau nhé
TN1 : 2HCl + Ba(OH)2 = BaCI2 + 2H2O
Gọi a là nồng độ mol/llít của ddA, b là nồng độ mol/lít của dd B, thí nghiệm 1 cho thấy dd thiếu là ddB (Ba(OH)2 ) từ đó kéo số mol dd Ba(OH)2 wa là 0,05b ra số mol dd A phản ứng là 0,1b mol.
HCl + NaOH = NaCl + H2O
từ số mol NaOH đề cho phản ứng với HCl dư là 0,1x0,05= 0,005 mol ta suy ra số mol HCl dư là 0,005 mol.
Như vậy tổng số mol HCl tham gia phản ứng trong TN 1 là 0,1b + 0,005 mol, ta có phương trình 0,1b + 0,005 = 0,05a
TN2 tương tự như vậy nhưng ở đây dd Ba(OH)2 là dd còn dư sau phản ứng,số mol dư là 0,07 mol ( kéo từ số mol HNO3 tham gia phản ứng ) ,như vậy tổng số mol Ba(OH)2 tham gia là 0,05a + 0,07 mol, ta có phương trình 0,05a + 0,07 = 0,15b giải hệ phương trình sẽ ra lần lượt a và b .
Đáp án B
Vì CH3COONa là chất điện li mạnh nên được viết trước để tạo môi trường cho cân bằng của chất điện li yếu phân li và cân bằng:
Cho mk hỏi là tại sao chỗ CH3COO là x+0,1 mà không phải là 0,1-x ạ , tại mk ko biết í