21.Thành phần khối lượng của hidro trong nước là:
A.11,1% B.66,7% C.50% D.33,3%
21-2:Thành phần khối lượng của oxi trong hợp chất Magie oxit MgO là:
A.20% B.40% C50% D.60%
21-3:Một hợp chất có thành phần (về khối lượng) của các nguyên tố:75% C, 25% H.Công thức của hợp chất đó là:
A.CH B.CH2 C.CH3 D.CH4
21-4:Một hợp chất có thành phần(về khối lượng) của các nguyên tố:24,4% Ca, 17,1% N,còn lại là O.Công thức của...
Đọc tiếp
21.Thành phần khối lượng của hidro trong nước là:
A.11,1% B.66,7% C.50% D.33,3%
21-2:Thành phần khối lượng của oxi trong hợp chất Magie oxit MgO là:
A.20% B.40% C50% D.60%
21-3:Một hợp chất có thành phần (về khối lượng) của các nguyên tố:75% C, 25% H.Công thức của hợp chất đó là:
A.CH B.CH2 C.CH3 D.CH4
21-4:Một hợp chất có thành phần(về khối lượng) của các nguyên tố:24,4% Ca, 17,1% N,còn lại là O.Công thức của hợp chất đó là(biết MCa=40g)
A.Ca(NO3)2 B.Ca(NO4)2 C.Ca(N2O2)2 D.CaNO3
21-5:Đốt nóng hỗn hợp magie và lưu huỳnh , thu được hợp chất là magie sunfua.Biết 2 nguyên tố kết hợp vs nhau theo tỉ lệ khối lượng là 3 phần Magie vs 4 phần lưu huỳnh
a)công thức hóa học đơn giản cùa magie sunfua là
A.MgS2 B.MgS C.Mg3S4 D.Mg2S
b)Nếu trộn 8 g lưu huỳnh rối đốt nóng , sản phẩm sau phản ứng có thành phần là :
A.7g magie sunfua B.8 g Magie C.16g Magie sunfua D.7g Magie sunfua vs 8g lưu huỳnh E.14g Magie và 2g Magie


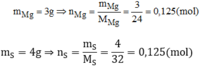
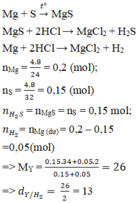
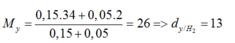

Giả sử hợp chất có khối lượng 7g → m M g = 3g ; m S = 4g
Chọn D. Vì:
Theo đề bài: 3g Mg kết hợp vừa đủ với 4g S.
Hoặc 6g Mg kết hợp vừa đủ với 8g S.
Nếu trộn 8g Mg với 8g S thì sẽ sinh ra 14g MgS và còn dư 2g Mg.