Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{HCl}=\dfrac{200}{1000}.2=0,4\left(mol\right)\)
\(PTHH:Mg+2HCl--->MgCl_2+H_2\uparrow\left(1\right)\)
a. Theo PT(1): \(n_{Mg}=n_{H_2}=n_{MgCl_2}=\dfrac{1}{2}.n_{HCl}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,2.24=4,8\left(g\right)\\V_{H_2}=0,2.22,4=4,48\left(lít\right)\end{matrix}\right.\)
b. \(PTHH:2NaOH+MgCl_2--->Mg\left(OH\right)_2\downarrow+2NaCl\left(2\right)\)
Ta có: \(n_{NaOH}=\dfrac{\dfrac{20\%.100}{100\%}}{40}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,5}{2}>\dfrac{0,2}{1}\)
Vậy NaOH dư.
Theo PT(2): \(n_{Mg\left(OH\right)_2}=n_{MgCl_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Mg\left(OH\right)_2}=0,2.58=11,6\left(g\right)\)
a: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
200ml=0,2 lít
\(n_{HCl}=0.2\cdot22.4=4.48\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=2.24\left(mol\right)\)
\(\Leftrightarrow m_{H_2}=n_{H_2}\cdot M=2.24\cdot1=2.24\left(g\right)\)
\(n_{MgCl_2}=2.24\left(mol\right)\)
\(\Leftrightarrow n_{Mg}=2.24\left(mol\right)\)
\(\Leftrightarrow m_{Mg}=2.24\cdot24=53.76\left(g\right)\)

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right);n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
PTHH: \(Fe+S-^{t^o}\rightarrow FeS\)
Theo đề: 0,2...0,3
Lập tỉ lệ \(\dfrac{0,2}{1}< \dfrac{0,3}{1}\)=> Fe hết. S dư
=> Sau phản ứng hỗn hợp gồm S dư, FeS
=> \(n_{S\left(dư\right)}=0,3-0,2=0,1\left(mol\right)\)
S + H2SO4 → SO2 + H2O
2FeS + 10H2SO4 → Fe2(SO4)3 + 9SO2 + 10H2O
\(\Rightarrow m_{H_2SO_4}=\left(0,1+\dfrac{0,2.10}{2}\right).98=107,8\left(g\right)\)
\(V_{SO_2}=\left(0,1+\dfrac{0,2.9}{2}\right).22,4=22,4\left(l\right)\)
\(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{FeS}=0,1\left(mol\right)\)
3Ba(OH)2 + Fe2(SO4)3 → 2Fe(OH)3↓ + 3BaSO4↓ (*)
Fe(OH)3 ---to→ Fe2O3 + H2O (**)Theo PT (*) : \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe\left(OH\right)_3}=0,05\left(mol\right)\)
Theo PT (**): \(n_{Fe_2O_3}=2n_{Fe\left(OH\right)_3}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,1.160=16\left(g\right)\)

Đáp án C
Phần 1: Tác dụng vói dung dịch H2SO4 loãng gồm Al và FexOy nên n H 2 = 3 2 n Al ⇒ n Al = 0 , 02
Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn và hỗn hợp B tác dụng với dung dịch NaOH dư có H2 nên B có Fe, A12O3 và Al dư. Có n Al du = 2 3 n H 2 ( NaOH ) = 0 , 004 .
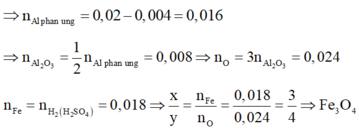

Đặt số mol Fe3O4 là x (mol)
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
x..............8x..........2x............x
Cu + 2FeCl3 ⟶ 2FeCl2 + CuCl2
x.........2x................2x.............x
Kim loại không tan là Cu
Dung dịch Y gồm FeCl2, CuCl2 và HCl dư
=> \(n_{FeCl_2}=x+2x=3x\left(mol\right);n_{CuCl_2}=x\left(mol\right)\)
\(n_{OH^-}=0,5.1+0,5.1=1\left(mol\right)\)
\(H^+_{\left(dư\right)}+OH^-\rightarrow H_2O\)
\(Fe^{2+}+2OH^-\rightarrow Fe\left(OH\right)_2\)
3x..........6x...............3x
\(Cu^{2+}+2OH^-\rightarrow Cu\left(OH\right)_2\)
x.............2x.................x
Kết tủa là Cu(OH)2 và Fe(OH)2
Ta có : \(3x.90+x.98=36,8\)
=> x=0,1 (mol)
=> \(m_{Cu}=x.64+1,6=8\left(g\right)\)
=> \(m=0,1.232+8=31,2\left(g\right)\)
Mặt khác : \(n_{HCl\left(dư\right)}=1-\left(6x+2x\right)=0,2\left(mol\right)\)
=> \(n_{HCl\left(bđ\right)}=8x+0,2=1\left(mol\right)\)

Đáp án B
Gọi a, b và c lần lượt là số mol của Mg, Fe3O4 và Fe(NO3)2.
Hỗn hợp khí Y gồm NO (0,07 mol) và H2 (0,03 mol).
Cho 8,66 gam X tác dụng với dung dịch hỗn hợp HCl và HNO3 thì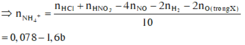
Cho Y tác dụng với NaOH, lọc kết tủa đun nóng thu được 10,4 gam hỗn hợp rắn gồm MgO (a mol) và Fe2O3 (1,5b + 0,5c) mol. Từ dữ kiện đề bài ta có hệ sau
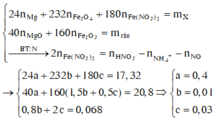

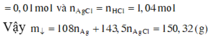







Đáp án:
m =32,4g
mddH2SO4 = 49g
Giải thích các bước giải:
a) MgCO3 + H2SO4 → MgSO4 + H2O +CO2 ↑
MgSO4 + 2NaOH → Mg(OH)2 + Na2SO4
$Mg{(OH)_2}\buildrel {to} \over
\longrightarrow MgO + {H_2}O$
b) nCO2 = 2,24 : 22,4 = 0,1mol
nMgCO3 = nCO2 = 0,1 mol
nMgO = 12:40=0,3mol
nMgSO4 = nMgO - nMgCO3 = 0,3 - 0,1 = 0,2mol
m = mMgCO3 + mMgSO4
= 0,1 .84+0,2.120=32,4g
nH2SO4 = nCO2 = 0,1 mol
mH2SO4 = 0,1.98=9,8g
mddH2SO4 = 9,8:20.100=49g
chúc bạn học tốt