Tính pH của dung dịch axit HCOOH 0,1M. Biết hằng số axit của axit fomic là 10-3,75
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Sửa đề bài Vì CH3COONa là chất điện li mạnh nên được viết trước để tạo môi trường cho cân bằng của chất điện li yếu phân li và cân bằng:
CH³COOH ⇔ CH³COO -+H+
Ban đầu 0,1 0. 0
Phân li xM x. x
Cân bằng 0,1-x 0,1+x x
Suy ra K = \(\dfrac{x(x+0,1)}{0,1-x}\) = 1,8.10 mũ âm ⁵
⇒ x = 1,8 . 10 mũ âm ⁵
⇒pH = log x = 1745

HD:
HA: 0,01 mol; NaOH: 0,005 mol.
Dung dịch B dư HA 0,005 mol.
HA \(\Leftrightarrow\) H+ + A-
bđ: 0,005 0 0
cb: 0,005-x x x
Ka = x2/(0,005-x) = 10-3,75.
Giải phương trình thu được x = 8,58.10-4 = [H+]. Do đó: pH = -log[H+] = 3,066.

Trước khi pha loãng: pH = 3 → [H+] = 10-3 → nH+ = 10-3V1 (mol).
Sau khi pha loãng: nH+ = 10-pHV2 (mol) = 10-pH .10V1 (mol)
Do số mol sau pha loãng > trước pha loãng nên: pH < 4

HNO2→H+ + NO2-
ban đầu 0,1..........0...........0
phân li x............x............x
cân bằng 0,1-x......x............x
\(Ka=\dfrac{\left[H^+\right]\left[NO_2^-\right]}{\left[HNO_2\right]}\\ 5.10^{-4}=\dfrac{x^2}{0,1-x}\)
\(\Rightarrow\left[H^+\right]=x=....\)
Em có thể tham khảo lí thuyết vào bài tập thêm trong chủ đề này
https://hoc24.vn/ly-thuyet/gia-tri-ph-cua-cac-dung-dich-axit-bazo.4749/

Khối lượng của 1 lít (1000 ml) dung dịch axit fomic 0,092% là 1000 g. trong đó khối lượng của axit fomic là:
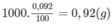
và số mol axit fomic là : 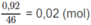
Số mol axit fomic phân li thành ion là:
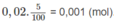
HCOOH ↔ H C O O - + H +
0,001 mol 0,001 mol
Nồng độ [ H + ] = 0,001 mol/l = 1. 10 - 3 mol/l. Vậy pH = 3.

Gọi x là nồng độ CH3COOH phân li.
\(\begin{matrix}CH_3COONa&\rightarrow&CH_3COO^-+&Na^+&\\0,08&&0,08&0,08&\left(M\right)\\CH_3COOH&\rightarrow&CH_3COO^-&+H^+&k_a=1,8.10^{-5}\\\begin{matrix}BD&0,1\end{matrix}&&0,08&&\\\begin{matrix}PU&x\end{matrix}&&x&x&\left(M\right)\\\begin{matrix}CB&0,1-x\end{matrix}&&0,08+x&x&\end{matrix}\)
\(k_a=\dfrac{\left[CH_3COO^-\right]\left[H^+\right]}{\left[CH_3COOH\right]}=\dfrac{\left(0,08+x\right)\left(x\right)}{\left(0,1-x\right)}=1,8.10^{-5}\)
\(x\approx2,24886.10^{-5}\)\(\Rightarrow pH=-log\left(\left[H^+\right]\right)=-log\left(x\right)=-log\left(2,24886.10^{-5}\right)\approx4,46804\)

Đáp án B
- Đầu tiên cho quỳ tím vào:
+ axit glutamic, HCOOH: màu đỏ
+ glyxin, NaI: không đổi màu.
+ Lysin: màu xanh → nên nhận biết được lysin.
- Cho tiếp A g N O 3 / N H 3 vào 2 nhóm chưa nhận được:
+ Nhóm axit: có kết tủa là HCOOH, còn lại là axit glutamic.
+ Nhóm không làm quỳ đổi màu: Có kết tủa vàng đậm là NaI (kết tủa AgI màu vàng); còn lại là glyxin

