giải giúp em câu này: cho 8,3g hai kim loại kiềm kế tiếp nhau tác dụng với 100g dd HCl 3,65% thu được dd X. Cho MgCl2 dư vào dd X thì thu được 4,35g kết tủa .Hai kim loại đó là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
![]()
nAgCl = 18,655/143,5 = 0,13
⇒ M= 6,645/ 0,13 - 35,5 = 15,61
⇒ M1 = 9 (Li) < 15,61 < M2 = 23(Na)

Sửa đề : 336 ml
Gọi: 2 kim loại là : M
nH2 = 0.015 mol
M + H2O --> MOH + 1/2H2
____________0.03____0.015
MOH + HCl --> MCl + H2O
0.03__________0.03
M = 2.075/0.03 =69.17
<=> M + 35.5 = 69.17
=> M = 33.67
Kim loại cần tìm là : K và Na
% bạn tự gọi số mol và giải phương trình nhé

Gọi kim loại kiềm thổ chung là R.
\(R+2HCl\rightarrow RCl_2+H_2\)
0,25 0,25
\(\Rightarrow M_R=\dfrac{8,15}{0,25}=32,6\)
\(\Rightarrow R_1< 32,6< R_2\)
Mà hai kim loại nằm ở 2 chu kì liên tiếp nên:
\(\left\{{}\begin{matrix}R_1:24\left(Mg\right)\\R_2:40\left(Ca\right)\end{matrix}\right.\)

MCl + AgNO3 -> AgCl + MNO3 (M là hai kim loại kiềm)
mol: 0,13 0,13
Ta có : (M+35,5).0,13 = 6,645
=> M = 15,62
Hai kim loại kiềm trên là Li và Na.
=> Đáp án D

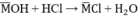
Theo pt: nHCl = nMOH = 0,1 (mol)
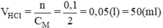
m(MCl) = 0,1.(31 + 35,5) = 6,65(g)

Đáp án : C
+) TH1 :Nếu tạo ra số mol OH bằng nhau
=> nX = nY => 17,55/X = 14,95/Y
=> X : Y = 27 : 23
=>Không có chất thỏa mãn
+) TH2 : Nếu với X thì Al3+ dư còn Y thì kết tủa hòa tan 1 phần
=> nAl(OH)3 = 1/3 nX = 5,85/X < 0,2 => X > 29,25g
Và y = 4.0,2 – 14,95/Y = 5,85/X
Nếu X = 39 => Y = 23g (Na) => nAl(OH)3 = 0,15 mol
=> y = 11,7g (có đáp án thỏa mãn)

Đáp án C
Hướng dẫn Ta có: ![]()
![]() Cl + AgNO3 →
Cl + AgNO3 → ![]() NO3 + AgCl
NO3 + AgCl
0,13 mol 0,13 mol
=> (![]() + 35,5).0,13 = 6,645 →
+ 35,5).0,13 = 6,645 → ![]() = 15,62
= 15,62
Mà 2 kim loại kiềm thuộc hai chu kì kế tiếp nhau → Li (7) và Na(23)

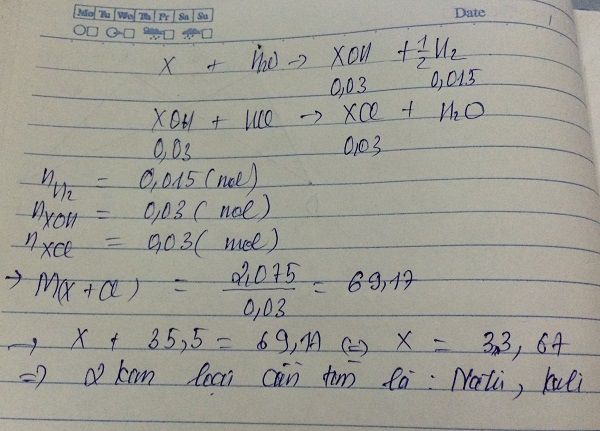





chả hiểu cái gì
trong SGK có bài này mà hình như mik lm òi