Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni.
Nung bình → hhX có dX/H2 = 8.
Theo BTKL: mhhX = mhh ban đầu = 0,35 x 26 + 0,65 x 2 = 10,4 gam
→ nhhX = 10,4 : 16 = 0,65 mol.
→ nH2phản ứng = nhh ban đầu - nX = 0,35 + 0,65 - 0,65 = 0,35 mol.
Ta có: nπ trước phản ứng = 2 x nCH≡CH = 2 x 0,35 = 0,7 mol.
→ nπ dư = nπ trước phản ứng - nH2 = 0,7 - 0,35 = 0,35 mol.
• Ta có nπ dư = 2 x nAgC≡CAg + nBr2
→ nBr2 = 0,35 - 2 x (12 : 240) = 0,25 mol

Đáp án : B
Theo BTKL: mX = 0,04 x 26 + 0,03 x 40 + 0,8 x 2 = 24 gam → nX = 24 : 24 = 1 mol.
Ta có nH2phản ứng = nhh ban đầu - nX = (0,4 + 0,3 + 0,8) - 1 = 0,5 mol.
nπ trước phản ứng = 2 x nCH≡CH + 2 x nCH≡C-CH3 = 2 x 0,4 + 2 x 0,3 = 1,4 mol.
→ nπ dư sau phản ứng = nπ trước phản ứng - nH2 = 1,4 - 0,5 = 0,9.
Mà nπ dư sau phản ứng = 2 x n↓ + nBr2 → n↓ = (0,9 - 0,1) : 2 = 0,4 mol.
Giả sử số mol của AgC≡CAg và AgC≡C-CH3 lần lượt là x, y mol
Ta có hpt: ![]()
→ m = 0,15 x 240 + 0,25 x 147 = 72,75 gam → Chọn C

Đáp án A
Gọi x, y, z, t lần lượt là số mol của C3H6, C4H10, C2H2 và H2 trong m gam X.
Do Y có phản ứng với dung dịch brom nên H2 hết, ta có:
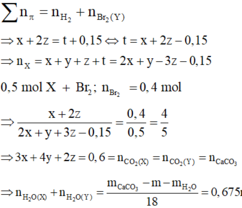
mX = mY = mC +mH = 8,55 gam
Theo định luật bảo toàn nguyên tố, ta có:
![]()

$C_2H_2+2H_2\xrightarrow{t^o,Ni}C_2H_6(1)$
$C_2H_2+2AgNO_3+2NH_3\to C_2Ag_2\downarrow+NH_4NO_3(2)$
$C_2H_2+2Br_2\to C_2H_2Br_4(3)$
$2C_2H_6+7O_2\xrightarrow{t^o}4CO_2+6H_2O$
Theo PT:
$n_{C_2H_2(2)}=n_{C_2Ag_2}=\frac{24}{240}=0,1(mol)$
$n_{C_2H_2(3)}=\frac{1}{2}n_{Br_2}=\frac{1}{2}.\frac{40}{160}=0,125(mol)$
$n_{C_2H_6}=\frac{1}{3}n_{H_2O}=\frac{1}{3}.\frac{11,7}{18}=\frac{13}{60}(mol)$
Sau pứ (1):
$n_{C_2H_2(dư)}=0,125+0,1=0,225(mol)$
Theo PT(1): $n_{C_2H_2(pứ)}=\frac{13}{60}(mol);n_{H_2}=\frac{13}{30}(mol)$
$\to a=n_{C_2H_2}+n_{H_2}=\frac{13}{60}+\frac{13}{30}+0,225=\frac{7}{8}(mol)$

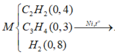
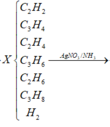
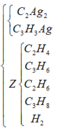
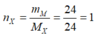
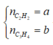
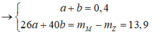
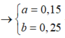
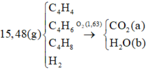
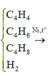
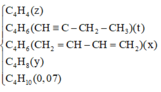
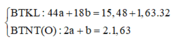
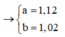
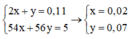
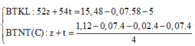
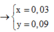
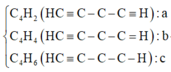
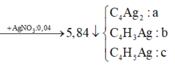
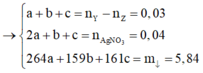
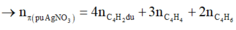
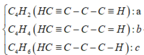
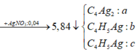
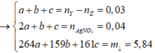

Đáp án : B
C2H2 → N H 4 C l , C u C l 2 CH≡C-CH=CH2 + C2H2 dư
Gọi số mol C2H2 ban đầu là x,
Với H= 60% nên số mol C4H4 là x . 0 , 6 3 = 0,2x mol, số mol C2H4 dư là 0,4x
Khi tham gia phản ứng với AgNO3/NH3 sinh ra kết tủa chứa CAg≡C-CH=CH2: 0,3x mol; CAg≡ CAg : 0,4 x mol
→ 159. 0,3x + 0,4x . 240 = 43,11 → x = 0,3 mol
Vậy ∑ m = 0,3. 26 = 7,8 gam. Đáp án B