Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a/
+ CO
- %mC = \(\frac{12}{12+16}.100\%=42,86\%\)
- %mO = 100% - 42,86% =57,14%
+CO2
- %mC = \(\frac{12}{12+16.2}.100\%=27,27\%\)
- %mO = 100% - 27,27% = 72,73%
b/
+Fe3O4
- %mFe = \(\frac{56.3}{56.3+16.4}.100\%=72,41\%\)
- %mO = 100% - 72,41% = 27,59%
+ Fe2O3
- %mFe = \(\frac{56.2}{56.2+16.3}.100\%=70\%\)
- %mO = 100% - 70% = 30%
c/
+SO2
- %mS = \(\frac{32}{32+16.2}.100\%=50\%\)
- %mO = 100% - 50% = 50%
+ SO3
- %mS = \(\frac{32}{32+16.3}.100\%=40\%\)
- %mO = 100% - 40% = 60%

a) Với Fe3O4 thì Fe là 72,4% và O là 27,6%;
Với Fe2O3 thì Fe là 70% và O là 30%
b) Với SO2 thì S là 50% và O là 50%
Với SO3 thì S là 40% và O là 60%
c) mCu= \(\dfrac{80.80}{100}\)=64(g) ; mO=\(\dfrac{80.20}{100}\)=16(g)
nCu=\(\dfrac{64}{64}\)=1(mol) ; nO=\(\dfrac{16}{16}\)=1(mol)
Vậy CTHH của oxit đồng màu đen là: CuO
d) dA/H2=\(\dfrac{Ma}{2}\)=17 => MA=2.17=34(đvC)
H =\(\dfrac{5,88.34}{100}\)\(\approx\)2(đvC) ; S =\(\dfrac{94,12.34}{100}\)\(\approx\)32
=> CTHH của chất khí A là SH2

\(PTK_{CuO}=64+16=80\left(đvC\right)\)
\(\%m_{Cu}=\) \(\dfrac{64}{80}.100=80\%\)
\(\%m_O=100-80=20\%\)
\(PTK_{MgCO_3}=24+12+3.16=84\left(đvC\right)\)
\(\%m_{Mg}=\dfrac{24}{84}.100=28,57\%\)
\(\%m_C=\dfrac{12}{84}.100=14,28\%\)
\(\%m_O=\dfrac{3.16}{84}.100=57,14\%\)
các ý còn lại làm tương tự

Câu 1 :
\(M_{K_2CO_3}=39.2+12+16.3=138\left(dvC\right)\)
\(\%K=\dfrac{39.2}{138}.100\%=56,52\%\)
\(\%C=\dfrac{12}{138}.100\%=8,69\%\)
\(\%O=100\%-56,52\%-8,69\%=34,79\%\)
Còn lại cậu làm tương tự nhá

\(CaCO_3\\ \%m_{Ca}=\dfrac{40}{40+12+3.16}.100=40\%\\ \%m_C=\dfrac{12}{40+12+16.3}.100=12\%\\ \Rightarrow\%m_O=100\%-\left(40\%+12\%\right)=48\%\\ H_2SO_4\\ \%m_H=\dfrac{2.1}{2.1+32+4.16}.100\approx2,041\%\\ \%m_S=\dfrac{32}{2.1+32+4.16}.100\approx32,653\%\\ \%m_O=\dfrac{4.16}{2.1+32+4.16}.100\approx65,306\%\\ Fe_2O_3\\ \%m_{Fe}=\dfrac{56.2}{56.2+16.3}.100=70\%\\ \Rightarrow\%m_O=100\%-70\%=30\%\)
CaCO3
\(\%M_{\dfrac{Ca}{CaCO_3}}=\dfrac{40}{100}.100\%=40\%\)
\(\%M_{\dfrac{C}{CaCO_3}}=\dfrac{12}{100}.100\%=12\%\)
\(\%M_{\dfrac{O}{CaCO_3}}=100\%-\left(40\%+12\%\right)=48\%\)
H2SO4
\(\%M_{\dfrac{H_2}{H_2SO_4}}=\dfrac{2}{98}.100\%=2,04\%\)
\(\%M_{\dfrac{S}{H_2SO_4}}=\dfrac{32}{98}.100\%=32,65\%\)
\(\%M_{\dfrac{O}{H_2SO_4}}=100\%-\left(2,04\%+32,65\%\right)=65,31\%\)
Fe2O3
\(\%M_{\dfrac{Fe}{Fe_2O_3}}=\dfrac{112}{160}.100\%=70\%\)
\(\%M_{\dfrac{O}{Fe_2O_3}}=100\%-70\%=30\%\)

\(M_{Fe_3O_4}=56.3+16.4=232\left(\dfrac{g}{mol}\right)\)
\(\%Fe=\dfrac{56.3}{232}.100\%=72,4\%\)
\(\%O=\dfrac{16.4}{232}.100\%=27,862\%\)
tìm công thức hóa học của hợp chất có thàn phần các nguyên tố như sau:55,189%K; 14,623%P và còn lại là oxi.Biết 0,05 mol hợp chất có khối lượng là 10,6 gam

Câu a) dễ bạn tự làm được đúng không mình làm mẫu một câu nha
Theo bài ra , ta có :
\(M_{NaNO_3}=23+\left(14+16\times3\right)=85\)(g/mol)
Trong 1 mol NaNO3 có 1 mol nt Na, 1mol nt N , 3 mol nt O
Thành phần % của các nguyên tử có trong hợp chất NaNO3 là :
\(\%Na=\left(\frac{1\times23}{85}\right)\times100\%\approx27\%\)
\(\%N=\left(\frac{1\times14}{85}\right)\times100\%\approx16,5\%\)
\(\%O=100\%-\left(\%Na+\%N\right)=100\%\left(27+16,5\right)=56,5\%\)
Vậy .....
b) Gọi CTDC là : NxHy
Theo bài ra , ta có :
dhợp chất X/H2= \(\frac{M_{N_xH_y}}{M_{H_2}}=8,5\Rightarrow M_{N_xH_y}=8,5\times M_{H_2}=8,5\times2=17\)(g/mol)
Khối lượng của nguyên tố trong hợp chất là :
\(m_N=\frac{MN_xH_y}{100\%}\times\%N=\frac{17\times82,35\%}{100\%}\approx14\left(g\right)\)
\(m_H=\frac{MN_xH_y}{100\%}\times\%H=\frac{17\times17,65\%}{100\%}\approx3\left(g\right)\)
Số mol của mỗi nt trong 1 mol Hợp chất NxHy là :
\(n_N=\frac{m}{M}=\frac{14}{14}=1\left(mol\right)\)
\(n_H=\frac{m}{M}=\frac{3}{1}=3\left(mol\right)\)
Suy ra trong 1 mol phân tử NxHy có : 1 nguyên tử N , 3 nguyên tử H
Vậy CTHH là : NH3
Chúc bạn học tốt =))![]()

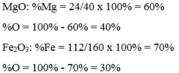

a) Hợp chất CO có MCO = 12 + 16 = 28 g/mol
%mO = 100 – 42,86 = 57,14%
Hợp chất CO2: có MCO2 = 12 + 32 = 44 g/mol
%mO = 100 – 27,3 = 72,7%
b) Hợp chất Fe3O4: MFe3O4 = 3.56 + 4.16 = 232 g/mol
%mO = 100 – 72,4 = 27,6%
Hợp chất Fe2O3: MFe2O3 = 2.56 + 3.16 = 160 g/mol
%mO = 100 – 70 = 30%
c) Hợp chất SO2 : MSO2 = 32 + 2.16 = 64 g/mol
%mO = 100 – 50 = 50%
Hợp chất SO3 : MSO3 = 32 + 16.3 = 80 g/mol
%mO = 100 – 40 = 60%