Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Điện phân trong 3378 giây tương đương với số e trao đổi là 0,07 mol
Do trao đổi 0,07 mol e chỉ thu được thêm 0,025 mol Cu, chứng tỏ Cu hết
Lúc này ở catot thu thêm 0,025 mol Cu và 0,01 mol H2
Vậy lúc này ở anot thu được thêm 0,025 mol khí
Do số mol khí trao đổi 0,07 nên chứng tỏ đã có tạo ra O2.
Vậy ở anot thu được Cl2 và O2 với số mol lần lượt là 0,015 và 0,01 mol.
Mặt khác do lúc t giây chỉ thu được Cu ở catot và Cl2 ở anot nên a=b.
Vậy t giây thì n e = 2 a nên 2t giây thì n e = 4 a
Lúc 2t giây ở anot thu được a+0,025 mol Cu và a-0,025 mol H2.
Ở catot thu được a+0,015 mol Cl2 và O2 0,5a-0,0075 mol
Tổng số mol khí thu được là: a-0,025+a+0,015+0,5a-0,0075=2,0625a
Giải được a= 0,04
Vậy số mol CuSO4 là 0,065 mol và KCl là 0,11 mol
=> m=18,595 gam

Chọn C
Do khi ta điện phân tiếp mà khối lượng catot vẫn tiếp tục tăng chứng tỏ ở t (s) thì Cu2+ chưa điện phân hết
Tại t (s):
Catot: Cu2+ + 2e → Cu
0,16 ←0,08
Tiếp tục điện phân tiếp 2t (s) nghĩa là tại 3t (s):
Catot:
Cu2+ + 2e → Cu
0,36 ←0,18
2H2O + 2e → 2OH- + H2.
Anot: 2Cl- → Cl2 + 2e
2x x 2x
2H2O → 4H+ + O2 + 4e
2y→4y → y→ 4y
Tại t = 3t (s) thì số mol e trao đổi gấp 3 lần tại t(s)
→ n(e trong quá trình tạo H2) = 0,16. 3 – 0,36 = 0,12 → n(H2) = 0,06
BT e: 2x + 4y = 0,48
Tổng số mol khí: x + y + 0,06 = 0,28
→ x = 0,2 và y = 0,02 → m = 0,18. 160 + 0,4. 74,5 = 58,6 (g)

Chọn đáp án C.
Phương trình điện phân:
Catot: C u 2 + + 2 e → C u
![]()
![]()
· Điện phân t giây:
m C u = m c a t o t = 5 , 12 g
⇒ n C u 2 + p h ả n ứ n g = 0 , 08 m o l
· Điện phân 3t giây:
m C u = 11 , 52 g ⇒ n C u 2 + = 0 , 18 m o l
⇒ n H 2 = 2 . 3 . 0 , 08 - 2 . 0 , 18 2 = 0 , 06 m o l
⇒ n C l 2 + n O 2 = 6 , 272 22 , 4 - 0 , 06 = 0 , 22 m o l 2 n C l 2 + 4 n O 2 = 6 . 0 , 08 = 0 , 48 m o l
⇒ n C l 2 = 0 , 2 m o l n O 2 = 0 , 02 m o l
![]()

Đáp án A
Do khi ta điện phân tiếp mà khối lượng catot vẫn tiếp tục tăng chứng tỏ ở t (s) thì Cu2+chưa điện phân hết
Tại t (s):
Catot: Cu2+ + 2e → Cu
0,16 ←0,08
Tiếp tục điện phân tiếp 2t (s) nghĩa là tại 3t (s):
Catot:
Cu2+ + 2e → Cu Anot: 2Cl- → Cl2 + 2e
0,36 ←0,18 2x x 2x
2H2O + 2e → 2OH- + H2. 2H2O → 4H+ + O2 + 4e
2y→4y → y→ 4y
Tại t = 3t (s) thì số mol e trao đổi gấp 3 lần tại t(s)
→ n(e trong quá trình tạo H2) = 0,16. 3 – 0,36 = 0,12 → n(H2) = 0,06
BT e: 2x + 4y = 0,48
Tổng số mol khí: x + y + 0,06 = 0,28
→ x = 0,2 và y = 0,02 → m = 0,18. 160 + 0,4. 74,5 = 58,6 (g)


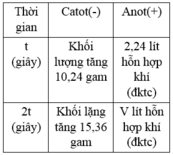
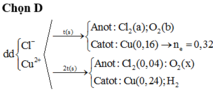
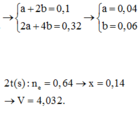
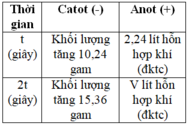
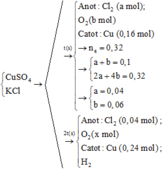
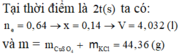

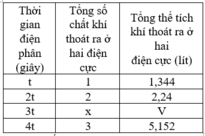

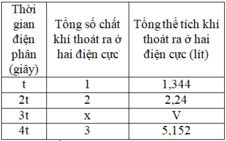



Đáp án B
2t(s): n e = 0,64 => x= 0,14=> V= 4,032