
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, nFe= \(\dfrac{28}{56}=0,5\) mol
nCu= \(\dfrac{64}{64}=1\) mol
nAl= \(\dfrac{5,4}{27}=0,2\) mol
b, VCO2= 0,175.22,4= 3,92 (l)
VH2= 1,25.22,4= 28 (l)
VN2= 3.22,4= 67,2 (l)
c, mA= \(\dfrac{12,25}{0,125}=98\) (g/mol)

CTHH sai: \(FeSO_4;NáSO_4;K\left(OH\right)_2\)
Sửa: \(Fe_3\left(SO_4\right)_3;Na_2SO_4;KOH\)

Mg2O sai
theo quy tắc hóa trị, oxi hóa trị 2, mg hóa trị 2, vậy CTHH là MgO

Xét các công thức hóa học (dựa vào hóa trị đã cho)
- MgCl Theo quy tắc hóa trị ta có: II.1 ≠ 1.I ⇒ Công thức MgCl sai
Gọi công thức dạng chung là 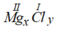
Theo quy tắc hóa trị ta có II.x= I.y ⇒ 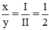 ⇒ x = 1, y = 2
⇒ x = 1, y = 2
⇒ Công thức đúng là MgCl2
- KO Theo quy tắc hóa trị ta có: I.1 ≠ II.1 ⇒ Công thức KO sai
Gọi công thức dạng chung là 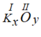
Theo quy tắc hóa trị ta có I.x= II.y ⇒ 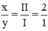 ⇒ x = 2, y = 1
⇒ x = 2, y = 1
⇒Công thức đúng là K2O
- CaCl2 Theo quy tắc hóa trị ta có: II.1 = I.2 ⇒ Công thức CaCl2 đúng
- NaCO3 Theo quy tắc hóa trị ta có: I.1 ≠ II.1 ⇒ Công thức Na2CO3 sai
Gọi công thức dạng chung là Nax(CO3)y
Theo quy tắc hóa trị ta có I.x = II.y ⇒ 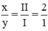 ⇒ x = 2, y = 1
⇒ x = 2, y = 1
⇒ công thức đúng là Na2CO3

CTHH sai và sửa lại:
HO → H2O
CaOH → Ca(OH)2
Fe2O → FeO hoặc Fe2O3 hoặc Fe3O4
NaO → Na2O
K2NO3 → KNO3
Ca2(PO4)3 → Ca3(PO4)2
Phần giải thích bạn xem lại quy tắc hóa trị để tự giải thích nhé.

\(Mg_2O\rightarrow MgO\)
\(Na_2\left(NO_3\right)_3\rightarrow NaNO_3\)
\(Na_2HCO_3\rightarrow NaHCO_3\)
\(CO_3\rightarrow CO_2\)
\(Ca_3PO_4\rightarrow Ca_3\left(PO_4\right)_2\)
\(KHSO_4\) (đúng)
\(SO_4\) (đúng)
\(H_2CO_3\) (đúng)
\(Ca\left(HSO_3\right)_2\) (đúng)
\(K\left(OH\right)_2\rightarrow KOH\)
\(ZnNO_3\rightarrow Zn\left(NO_3\right)_2\)
\(BaHS\rightarrow Ba\left(HSO_3\right)_2\)
Vẫn có muối của \(Ba^{^{ }2+},HS^{^{ }-}\) bạn nhé. Dù công thức đó sai, CT đúng là \(Ba\left(HS\right)_2\), nhưng bạn sửa thành một hợp chất hoàn toàn khác là trái yêu cầu đề nhé.


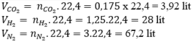

Bài 3:
a, Gọi: \(\left\{{}\begin{matrix}n_{Zn}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\) ⇒ 65x + 56y = 14,9 (g) (1)
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{H_2SO_4}=n_{Zn}+n_{Fe}=x+y=2.0,125=0,25\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,1\left(mol\right)\\n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,1.65=6,5\left(g\right)\\m_{Fe}=0,15.56=8,4\left(g\right)\end{matrix}\right.\)
b, Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,25\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: \(n_{CuO}=n_{H_2}=0,25\left(mol\right)\Rightarrow m_{CuO}=0,25.80=20\left(g\right)\)