Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nêu phương pháp hoá học để phân biệt 3 chất lỏng riêng biệt: xăng, rượu etylic và axit axetic.
ta nhúm quỳ
Quỳ chuyển đỏ :CH3COOH
Quỳ ko chuyển màu : xăng, rượu etylic
Ta có thể ngưởi mùi :
-Mùi hắc, dễ bay hơi :xăng
- còn lại rượu etylic
Có các bình đựng khí riêng biệt: CO2, Cl2, CO, H2. Hãy nhận biết các khí trên bằng phương pháp hoá học, viết phương trình nếu có
ta nhúm quỳ ẩm
-Quỳ chuyển màu rồi mất màu : Cl2
-Quỳ chuyển màu đỏ nhạt :CO2
ko hiện tg :CO,H2
Ta đốt :
-Chất cháy mà có tiếng nổ , lửa xanh nhạt :H2
-Còn lại là CO
2CO+O2->2CO2
2H2+O2-to>2H2O
Cl2+H2O->HCl+HClO
CO2+H2O->H2CO3

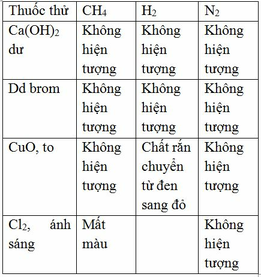
Đốt các khí:
Khí không cháy là oxi, khí cháy tạo ra CO 2 (nhận được nhờ dung dịch Ca OH 2 ) là CH 4 . Khí còn lại là H 2

Nhận ra CO 2 nhờ dung dịch Ca OH 2 , phân biệt CH 4 và H 2 tương tự câu a.

Đốt các khí. Khí không sinh ra CO 2 là H 2 . Hai khí cháy sinh ra CO 2 đó là CH 4 và CO.
Làm lạnh sản phẩm cháy khi đốt CH 4 và CO, trường hợp nào sinh ra H 2 O, đó là CH 4 . Khí con lại là CO.

2.-Trích mỗi lọ một ít làm mẫu thử
-cho Cu tác dụng từng chất, nhận ra HNO3 có khí không màu hóa nâu trong không khí(NO).Nhận ra AgNO3 và HgCl2 vì pư tạo dung dịch màu xanh.
-Dùng dung dịch muối Cu tạo ra, nhận ra được NaOH có kết tủa xanh lơ.
Dùng Cu(OH)2 để nhận ra HCl làm tan kết tủa.
-Dùng dd HCl để phân biệt AgNO3 và HgCl2 ( có kết tủa trắng là AgNO3 )
PTHH:3Cu + 8HNO3 -->3Cu(NO3)2 + 4H2O + 8NO
2AgNO3 + Cu --> 2Ag + Cu(NO3)2
Cu + HgCl2 --> CuCl2 + Hg
NaOH + Cu(NO3)--> Cu(OH) + NaNO3
Cu(OH)2 + 2HCl--> CuCl2 + 2H2O
AgNO3 +HCl--> AgCl+ HNO3
1) * Trích mỗi ống nghiệm một ít hóa chất đánh dấu làm mẫu thử
- Cho một mẩu quỳ tím vào 3 mẫu thử
+ Nếu dung dịch nào làm quỳ tím ngả màu xanh là dung dich HCl
+ Nếu mẫu thử làm cho quỳ tím ngả màu đỏ là dung dịch H2SO4
- Còn lại là HNO3

- Cho các khí tác dụng với giấy quỳ tím ẩm:
+ Không hiện tượng: C2H2, CH4 (1)
+ QT chuyển đỏ: SO2, HCl (2)
\(SO_2+H_2O\rightarrow H_2SO_3\)
- Dẫn khí ở (1) qua dd Br2 dư:
+ Không hiện tượng: CH4
+ dd nhạt màu dần: C2H2
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
- Dẫn khí ở (2) qua dd Br2 dư:
+ Không hiện tượng: HCl
+ dd nhạt màu: SO2
\(SO_2+Br_2+2H_2O\rightarrow H_2SO_4+2HBr\)

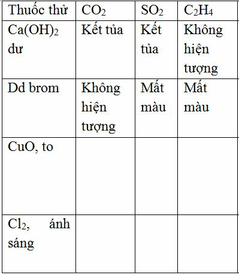
Dẫn qua dd Ca(OH)2 dư:
- CO2 bị hấp thụ
- Còn lại ko hiện tượng
Dẫn qua dd Br2 dư:
- C2H2 làm mất màu Br2 và có kết tủa màu vàng
- C2H4 làm mất màu Br2
- CH4 không làm mất màu Br2

Thí nghiệm 1 : Dẫn các khí qua ống thuỷ tinh vuốt nhọn rồi đốt. Hai khí cháy được là CH 4 và C 2 H 2 . Khí không cháy được là SO 2
Thí nghiệm 2 : Dẫn hai khí “cháy được” qua dung dịch brom Khí nào làm mất màu dung dịch brom, đó là C 2 H 2 , khí còn lại là CH 4


Dẫn lần lượt các khí qua dung dịch AgNO3/NH3 :
- Kết tủa vàng : C2H2
Hai khí còn lại sục vào dung dịch Ca(OH)2 dư :
- Kết tủa trắng : SO2
- Không HT : CH4
C2H2 + 2AgNO3 + 2NH3 => Ag2C2 + 2NH4NO3
Ca(OH)2 + SO2 => CaSO3 + H2O