Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức oxit sắt cần tìm là F e X O Y
Theo bài ta có: : = 7 : 3
Ta coi m F e = 7 gam; m O = 3 gam.
Khi đó:
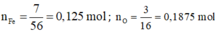
⇒ m C a O H 2 = 2.(40+17.2) = 148kg
⇒ n F e : n O = x : y = 0,125 : 0,1875 = 2 : 3
Vậy oxit sắt cần tìm là F e 2 O 3
⇒ Chọn A.

a.3Fe + 2O2 → Fe3O4
Số nguyên tử Fe : số nguyên tử O2 : số phân tử Fe3O4 = 3:2:1
b.Áp dụng ĐLBTKL ta có: m Fe + m O2 = m Fe3O4 = 8,4 + 3,2 =11, 6 gam
-số mol Fe=0,15mol
-số mol O2=0,1mol
3Fe+2O2\(\rightarrow\)Fe3O4
Tỉ lệ; số nguyên tử Fe:số phân tử O2: số phân tử Fe3O4=3:2:1
Tỉ lệ:\(\dfrac{0,15}{3}=\dfrac{0,1}{2}=0,05\)nên 2 chất phản ứng vừa đủ với nhau nên sản phẩm tính theo 1 trong 2 chất tham gia hoặc BTKL:
BtKL: moxit=8,4+3,2=11,6g

Câu 1 :
\(CT:Fe_xO_y\)
\(\%O=100-70=30\%\)
\(\dfrac{\%Fe}{\%O}=\dfrac{56x}{16y}=\dfrac{70}{30}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:Fe_2O_3\)

a) PTHH: \(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\left(1\right)\)
Ta có: \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
\(\Rightarrow n_{O_2}=2.0,03=0,06\left(mol\right)\)
\(\Rightarrow n_{Fe}=3.0,03=0,09\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,09.56=5,04\left(mol\right)\)
b) PTHH: \(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
Ta có: \(n_{O_2\left(2\right)}=n_{O_2\left(1\right)}=0,06\left(mol\right)\)
\(\Rightarrow n_{KMnO_4}=2.0,06=0,12\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,12.158=18,96\left(g\right)\)

1) nAgCl = 0,03 mol = nCl trong muối sắt
=> mCl = 1,065g => mFe = m muối - mCl = 1,625 - 1,065 = 0,56g
=> nFe = 0,01 mol
nFe : nCl = 1:3 => FeCl3
2) nOH- : nH3PO4 = 1,375 => muối tạo thành là NaH2PO4 và Na2HPO4
Gọi số mol NaH2PO4 và Na2HPO4 lần lượt là a, b. Ta có hệ:
bảo toàn Na: a + 2b = 0,0275
Bảo toàn P: a + b = 0,02
=> a, b

đặt CTHH của oxit sắt là FexOy
khi cho hỗn hợp X vào dd HCl dư thì chỉ có oxit sắt Pư còn Ag thì ko:
2 FexOy + 2y HCl ➝ FeCl2y/x + y H2O
do đó khối lượng oxit sắt ban đầu là: 80,8 - 11,2 = 69,6 (g)
khi cho ddA tác dụng với NaOH dư:
FeCl2y/x + (2y/x)NaOH ➝ Fe(OH)2y/x + (2y/x) NaCl
khi cho chất rắn vừa tạo ra đun nóng trong không khí:
2 Fe(OH)2y/x + 3/2 O2 ➝ Fe2O3 + 2y/x H2O
nhìn thì dài dòng nhưng bạn chỉ cần bảo toàn nguyên tố Fe cũng ra Ct đó
vì chất rắn nung trong không khì đến khối lượng ko đổi nên chất rắn là Fe2O3
nFe2O3= 72/160 = 0,45 (mol) ➩ nFe = 2 * 0,45 = 0,9(mol)
BTNT Fe: nFe ( FexOy) = nFe ( Fe2O3)
hay 69,6/ (56x+16y) * x = 2* 0,45
<=> 69,9x = 50,4x + 14,4y
<=> 19,2x = 14,4y
<=> x/y = 14,4/19,2 = 3:4
do đó CTHH của oxit là Fe3O4



Chọn B
Tỉ lệ khối lượng giữa Fe và O là 7/3
=> Đặt khối lượng của Fe là 7 thì khối lượng của O là 3