Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

M chiếm 46,67% về khối lượng:

Quan sát – phân tích: Hệ 5 ẩn gồm 4 phương trình không thể giải thông thường để tìm nghiện vì ta cần phải rút gọn nghiệm: Phương trình (2) chứa ẩn ZM và x. ZA từ phương trình (1); (3); (4) ta có thể đưa về 1 phương trình chứa 2 ẩn ZM và x
Z A → Đưa về hệ phương trình 2 ẩn.
Ta đưa được về hệ sau
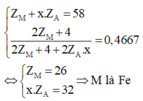
M là Fe nên x sẽ nhận giá trị từ 1 đến 3.
Từ x.ZA = 32 ta có các giá trị của ZA

Vậy H là FeS2
Đáp án A.

Câu 1,2
Cho nước vào hỗn hợp, lọc bỏ phần không tan
Cho thêm dung dịch CaCl2 tới dư vào, lọc bỏ phần không tan
$CaCl_2 + Na_2SO_4 \to CaSO_4 + 2NaCl$
$CaCl_2 + MgSO_4 \to CaSO_4 + MgCl_2$
Dung dịch gồm : NaCl,MgCl2,Na2SO4,CaCl2
Cho dung dịch NaOH dư vào, lọc bỏ phần không tan
$MgCl_2 + 2NaOH \to Mg(OH)_2 + 2NaCl$
Dung dịch gồm : NaCl,Na2SO4,NaOH,CaCl2
Cho thêm dung dịch H2SO4 tới dư vào, lọc bỏ phần không tan, cho bay hơi dung dịch
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$CaCl_2 + H_2SO_4 \to CaSO_4 + 2HCl$
Chất rắn khan gồm : Na2SO4,NaCl
Cho dung dịch BaCl2 tới dư vào, lọc dung dịch
$BaCl_2 + Na_2SO_4 \to BaSO_4 + 2NaCl$
Dung dịch gồm : BaCl2,NaCl
Cho dung dịch H2SO4 tới dư vào, cô cạn dung dịch . Ta được naCl tinh khiết
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
TK: nếu là 67 thì
1.1
M là Fe (26); A là S (16) công thức là FeS2
Giải thích các bước giải:
Ta có %M=46,67% -> %A=53,33%
Ta có : M=n+p; A=n'+p'
-> (n+p)/(x(n'+p'))=46,67/53,33=7:8
Vì n-p=4 -> n=4+p
-> (2p+4)/2xp'=7/8 -> 7xp'-8p=16
Tổng số proton =p+xp'=58 -> p=26; xp'=32
Vì A là phi kim thuộc chu kì 3 nên 15 <= p' <=17 (P; S; Cl)
Với x=2 -> p'=16
Vậy M là Fe; A là S công thức là FeS2
1.2
cho vào lượng dư dung dịch BaCl2
MgSO4+BaCl2=>BaSO4+MgCl2
lọc bỏ kết tủa tiếp tục cho vào lượng dư Na2CO3
MgCl2+Na2CO3=>MgCO3+2NaCl
BaCl2+Na2CO3=>BaCO3+2NaCl
CaCl2+Na2CO3=>CaCO3+2NaCl
lọc bỏ kết tủa, dung dịch gồm NaCl Na2CO3 dư
cho HCl dư vào
2HCl+Na2CO3=>2NaCl+H2O+CO2
đun nhẹ dung dịch cho HCl dư bay hơi cô cạn dung dịch thu được NaCl tinh khiết

Đáp án C
Tổng số proton trong MX2 là 58 hạt
→ ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt
→ -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX
= (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng
![]()
![]()
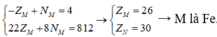
![]()
Cấu hình electron của M là [Ar]3d64s2.

Có lẽ đề hỏi cấu hình e của M bạn nhỉ?
Ta có: P = E (do nguyên tử trung hòa về điện)
- M chiếm 140/3% trong MX2
\(\Rightarrow\dfrac{P_M+N_M}{P_M+N_M+2P_X+2N_X}.100\%=\dfrac{140}{3}\%\) (1)
- Trong hạt nhân của M có số p ít hơn số n là 4.
⇒ NM - PM = 4 (2)
- Trong hạt nhân của X có số p bằng số n.
⇒ NX = PX (3)
- Tổng số p trong A là 58.
⇒ PM + 2PX = 58 (4)
Từ (1), (2), (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}P_M=26\\N_M=30\\P_X=16\\N_X=16\end{matrix}\right.\)
→ 1s22s22p63s23p63d64s2
→ Đáp án: C

Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng → ZM + NM =
7
15
. (116 + NM- ZM ) → 22ZM + 8NM = 812
Ta có hệ
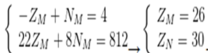
M là Fe
→ ZX =
58
-
26
2
= 16 → X là S
Công thức của A là FeS2.
Đáp án A.

Đáp án A
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM - ZM
M chiếm 46,67% về khối lượng
![]()
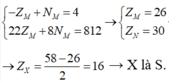
=> M là Fe

Chọn C
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số nơtron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số nơtron bằng số proton → ZX = NX
MH =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX = 58 + NM + 58 - ZM = 116 + NM - ZM


Giả sử: M số proton và nơtron lần lượt là p và n
=> Khối lượng nguyên tử của M: mp.p+mn.n
X có số p và n lần lượt là p và n
=> Khối lượng nguyên tử của X là: mp.p +mn.n
( mp và mn lần lượt là khối lượng của 1 hạt proton và 1 hạt nơtron)
Mà mp =mn = 1,67.10^-27 nên
Khối lượng nguyên tử của M: mp.( n+p)
Khối lượng nguyên tử của X : mp.(n + p )
(+++: Vì khối lượng của 1 nguyên tử là tổng khối lượng của p, e và n, mà khối lượng của e không đáng kể nên khối lượng của nguyên tử có thể tính bằng khối lượng của p và n)
* ta có:
n-p = 4 <=> n=p+4 (1)
n =p (2)
p+ xp = 58 => xp = 58 - p (3)
* Hợp chất A có công thức MX(x) trong đó M chiếm 46,67% về khối lượng nên:
M / (M+xX) = 46,67/100 <=> [mp.(n+p)] / [mp.(n+p) + x.mp.(n +p )] = 46,67/100
<=> (n+p) / [(n+p) +x(n +p )] = 46,67/100 (4)
Thay (1), (2), (3) vào (4) ta giải ra được : p = 26 => Kim loại M chính là Fe
p=26 => n= 26 +4 = 30 và xp = 32
Với x=1 => p =32 => phi kim là Ge (loại )
Với x=2 => p =16 => phi kim là S( thuộc chu kì 3 nên thỏa mãn điều kiên=> chọn)
Vậy công thức của hợp chất A là: FeS2


Đáp án D
Trong hợp chất MAx, M chiếm 46,67% về khối lượng nên :
Tổng số proton trong MAx là 58 nên: p + xp’ = 58. Từ đây tìm được: p = 26 và xp’ = 32.
Do A là phi kim ở chu kì 3 nên 15 ≤ p’ ≤ 17. Vậy x = 2 và p’ = 16 thỏa mãn.
Vậy M là Fe và A là S; công thức của MAx là FeS2.