Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 2:
\(m_{HF}=\dfrac{2,5.40\%}{100\%}=1(kg)\\ \Rightarrow n_{HF}=\dfrac{1}{20}=0,05(kmol)\\ PTHH:CaF+H_2SO_4\to CaSO_4+2HF\\ \Rightarrow n_{CaF}=0,025(kmol)\\ \Rightarrow m_{CaF}=0,025.78=1,95(kg)\)
Bài 3:
\(a,\) Đặt \(\begin{cases} n_{Fe}=x(mol)\\ n_{Al}=y(mol) \end{cases} \)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow \begin{cases} 56x+27y=11\\ x+1,5y=0,4 \end{cases} \Rightarrow \begin{cases} x=0,1(mol)\\ y=0,2(mol) \end{cases}\\ \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \%_{Al}=100\%-50,91\%=49,09\% \end{cases} \)
\(b,\Sigma n_{HCl}=3n_{Al}+2n_{Fe}=0,2+0,6=0,7(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,7}{2}=0,35(l)\)

Câu 5:
\(n_{Cl_2}=\dfrac{1120}{22,4}=50(mol)\\ PTHH:2KMnO_4+16HCl\to 2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\\ \Rightarrow n_{KMnO_4}=\dfrac{2}{5}n_{Cl_2}=20(mol)\\ \Rightarrow m_{KMnO_4}=20.158=3160(g)\)
Câu 6:
Đặt \(n_{Mg}=x(mol);n_{Al}=y(mol)\Rightarrow 24x+27y=10,2(1)\)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow x+1,5y=0,5(2)\\ (1)(2)\Rightarrow x=y=0,2(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,2.27}{10,2}.100\%=52,94\%\\ \Rightarrow \%_{Mg}=100\%-52,94\%=47,06\%\\ b,\Sigma n_{HCl}=3y+2x=1(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{1}{2}=0,5(l)\)

Quan sát phương trình phản ứng ta thấy S tăng từ mức oxi hóa +4 lên mức oxi hóa +6; Mn giảm từ mức oxi hóa +7 xuống mức oxi hóa +2 → SO2 là chất khử và KMnO4 là chất oxi hóa.
5 x S + 4 → S + 6 + 2 e
2 x M n + 7 + 5 e → M n + 2
Suy ra phương trình phản ứng đã cân bằng như sau:
5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
Chọn đáp án A.

So sánh ngũ ngôn cổ thể với ngũ ngôn hiện đại giúp mình với

I)
1) CuO + CO --to--> Cu + CO2
2) CO2 + Ca(OH)2 ---> CaCO3 + H2O
3) NaHCO3 + NaOH ---> Na2CO3 + H2O
4) Ca(HCO3)2 + 2KOH ---> CaCO3 + K2CO3 + 2H2O
II) \(n_{H_3PO_4}=0,05.1=0,05\left(mol\right)\)
PTHH: 2NaOH + H3PO4 ---> Na2HPO4 + 2H2O
0,1<----0,05--------->0,5
=> \(\left\{{}\begin{matrix}V=V_{ddNaOH}=\dfrac{0,1}{1}=0,1\left(l\right)=100\left(ml\right)\\m_{muối}=m_{Na_2HPO_4}=0,05.142=7,1\left(g\right)\end{matrix}\right.\)
III)
| NH4Cl | NaNO3 | NaBr | Cu(NO3)2 | |
| dd AgNO3 | - Kết tủa trắng | - Không hiện tượng | - Kết tủa vàng nhạt | - Không hiện tượng |
| dd NaOH | - Không hiện tượng | - Kết tủa xanh lơ |
NH4Cl + AgNO3 ---> AgCl + NH4NO3
NaBr + AgNO3 ---> AgBr + NaNO3
Cu(NO3)2 + 2NaOH ---> Cu(OH)2 + 2NaNO3
IV)
Gọi nCu = a (mol); nAl = b (mol)
=> 64a + 27b = 15 (1)
\(n_{NO}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Quá trình oxi hóa, khử:
Cu0 ---> Cu+2 + 2e
a---------------->2a
Al0 ---> Al+3 + 3e
b--------------->3b
N+5 + 3e ---> N+2
0,9<----0,9
BTe: 2a + 3b = 0,9 (2)
Từ (1), (2) => a = 0,15; b = 0,2
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,15.64}{15}.100\%=64\%\\\%m_{Al}=100\%-64\%=36\%\end{matrix}\right.\)

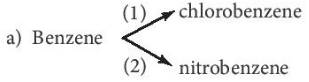
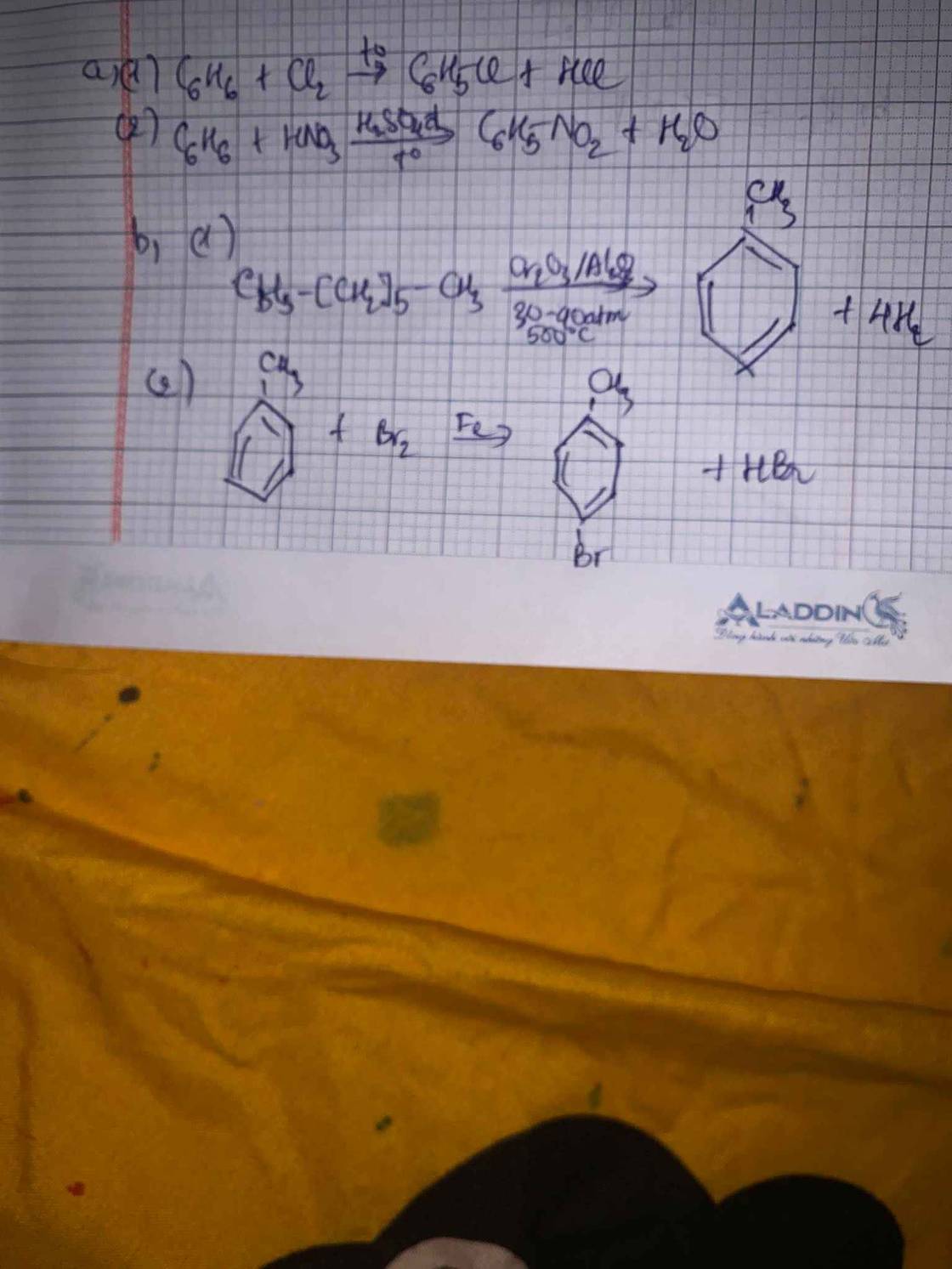
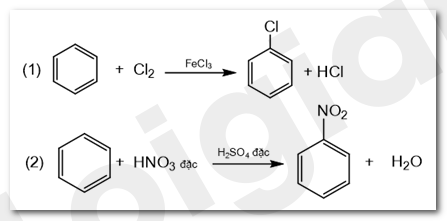
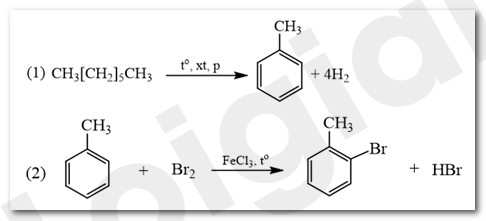

2H2SO4 + C => 2H2O + 2SO2 + CO2
C+2H2SO4→2H2O+2SO2+CO2