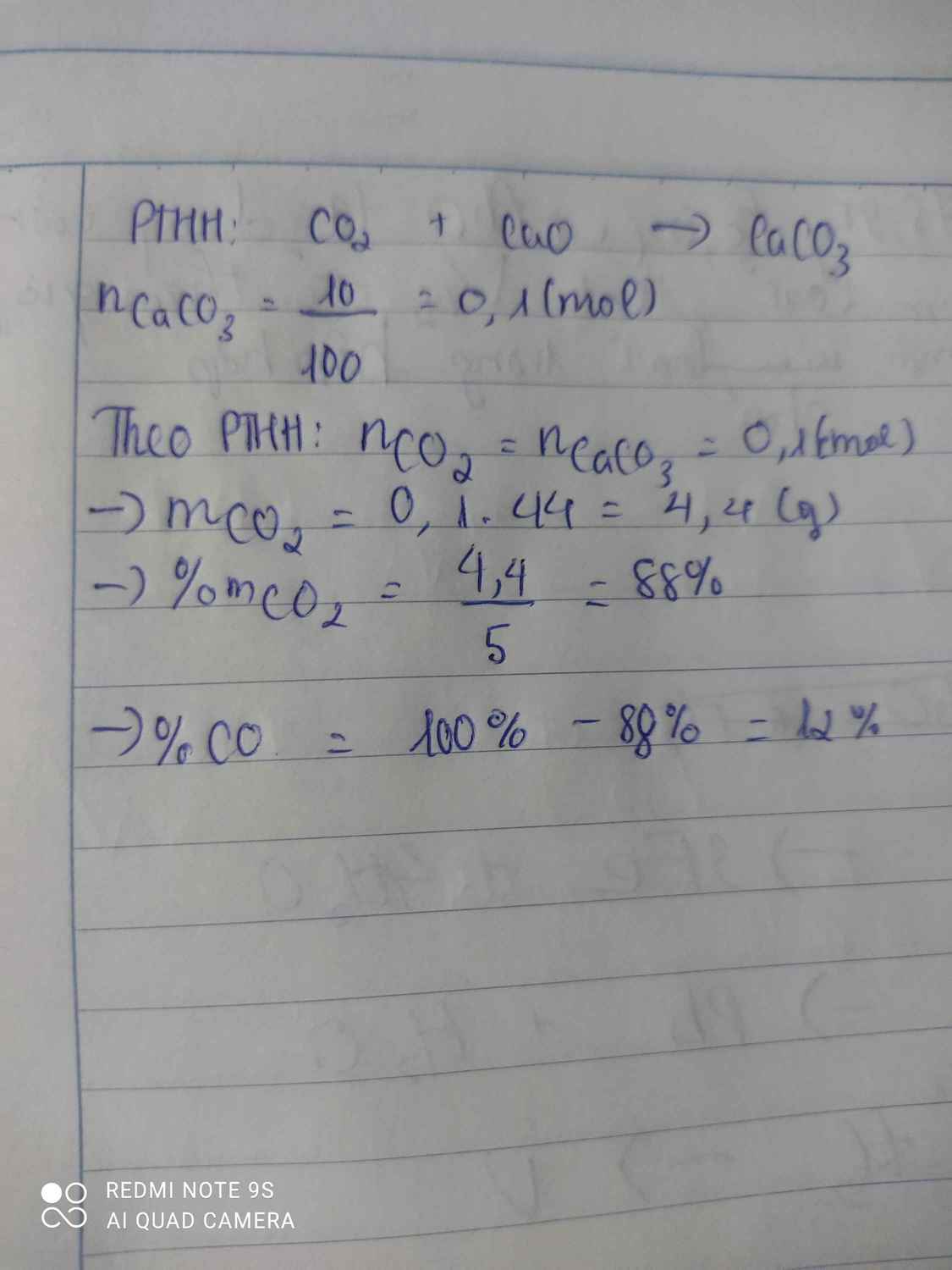Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{CaCO3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố C: \(n_{CO}=n_{CaCO_3}=0,02\left(mol\right)\)
\(n_{Cu}=\dfrac{1,92}{64}=0,03\left(mol\right)\)
CuO + CO -------> Cu + CO2
0,02-------->0,02-->0,02
CuO + H2 -------> Cu + H2O
0,01<--------0,03-0,02=0,01
Phần trăm về thể tích cũng là phần trăm về số mol
=>\(\%V_{H_2}=\dfrac{0,01}{0,01+0,02}.100=33,33\%\)
=> %VCO=100- 33,33=66,67%
\(\%m_{H_2}=\dfrac{2.0,01}{2.0,01+44.0,02}.100=2,22\%\)
%mCO= 100-2,22=97,78%
b) \(V_{CO_2}=0,02.22,4=0,448\left(l\right)\)

\(n_{Ba\left(ỌH\right)_2}=0,1.0,3=0,03\left(mol\right)\\ n_{BaCO_3}=\dfrac{3,94}{197}=0,02\left(mol\right)\)
PTHH:
Ba(OH)2 + CO2 ---> BaCO3 + H2O
0,02 0,02 0,02
So sánh: 0,2 < 0,3 => Có tạo muối axit
\(n_{Ba\left(OH\right)_2\left(tạo.muối.axit\right)}\) = 0,03 - 0,02 = 0,01 (mol)
Ba(OH)2 + CO2 + H2O ---> Ba(HCO3)2
0,01 0,01
=> nCO2 = 0,02 + 0,01 = 0,03 (mol)
PTHH: C + O2 ---to---> CO2
0,03 0,03 0,03
mC = 0,03.12 = 0,36 (g)
=> m = mthan = \(\dfrac{0,36}{100\%-4\%}=0,375\left(g\right)\)
Gọi nO2 (dư) = a (mol)
=> \(M_A=\dfrac{0,03.44+32a}{0,03+a}=19,6.2\\ \Leftrightarrow a=0,02\left(mol\right)\)
=> VO2 = (0,03 + 0,02).22,4 = 1,12 (l)

đề đáng lẽ phải là tính a với V1 chứ :v
\(\left\{{}\begin{matrix}n_{Ba\left(OH\right)_2}=0,3.0,1=0,03\left(mol\right)\\n_{KOH}=0,3.0,2=0,06\left(mol\right)\end{matrix}\right.\)
\(n_{BaCO_3}=\dfrac{3,94}{197}=0,02\left(mol\right)\)
- TH1: Kết tủa không bị hòa tan
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,02<----0,02
=> nCO2 = 0,02 (mol)
- Nếu trong hỗn hợp A chứa CO2, O2 dư
\(\overline{M}_A=\dfrac{0,02.44+32.n_{O_2}}{0,02+n_{O_2}}=19,6.2=39,2\left(g/mol\right)\)
=> nO2(dư) = \(\dfrac{1}{75}\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,02<-0,02<---0,02
=> \(V_1=\left(\dfrac{1}{75}+0,02\right).22,4=\dfrac{56}{75}\left(l\right)\)
\(m_C=0,02.12=0,24\left(g\right)\)
=> \(a=m_{than}=\dfrac{0,24.100}{96}=0,25\left(g\right)\)
- Nếu trong hỗn hợp chứa CO2, CO
\(\overline{M}=\dfrac{0,02.44+28.n_{CO}}{0,02+n_{CO}}=39,2\left(g/mol\right)\)
=> \(n_{CO}=\dfrac{3}{350}\left(mol\right)\)
Bảo toàn C: \(n_C=0,02+\dfrac{3}{350}=\dfrac{1}{35}\left(mol\right)\)
=> \(m_C=\dfrac{1}{35}.12=\dfrac{12}{35}\left(g\right)\)
Bảo toàn O: \(n_{O_2}=\dfrac{0,02.2+\dfrac{3}{350}}{2}=\dfrac{17}{700}\left(mol\right)\)
=> \(V_1=\dfrac{17}{700}.22,4=0,544\left(l\right)\)
TH2: Nếu kết tủa bị hòa tan 1 phần
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,03----->0,03---->0,03
2KOH + CO2 --> K2CO3 + H2O
0,06-->0,03---->0,03
K2CO3 + CO2 + H2O --> 2KHCO3
0,03--->0,03
BaCO3 + CO2 + H2O --> Ba(HCO3)2
0,01--->0,01
=> nCO2 = 0,1 (mol)
- Nếu trong A chứa CO2, O2 dư
\(\overline{M}_A=\dfrac{0,1.44+32.n_{O_2}}{0,1+n_{O_2}}=39,2\left(g/mol\right)\)
=> \(n_{O_2}=\dfrac{1}{15}\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,1<-0,1<------0,1
=> \(m_C=0,1.12=1,2\left(g\right)\)
=> \(a=m_{than}=\dfrac{1,2.100}{96}=1,25\left(g\right)\)
\(V_1=\left(\dfrac{1}{15}+0,1\right).22,4=\dfrac{56}{15}\left(l\right)\)
- Nếu trong A chứa CO2, CO
\(\overline{M}_A=\dfrac{0,1.44+28.n_{CO}}{0,1+n_{CO}}=39,2\left(g/mol\right)\)
=> \(n_{CO}=\dfrac{3}{70}\left(mol\right)\)
Bảo toàn C: \(n_C=0,1+\dfrac{3}{70}=\dfrac{1}{7}\left(mol\right)\)
=> \(m_C=\dfrac{1}{7}.12=\dfrac{12}{7}\left(g\right)\)
=> \(a=m_{than}=\dfrac{\dfrac{12}{7}.100}{96}=\dfrac{25}{14}\left(g\right)\)
Bảo toàn O: \(n_{O_2}=\dfrac{2.0,1+\dfrac{3}{70}}{2}=\dfrac{17}{140}\left(mol\right)\)
=> \(V_1=\dfrac{17}{140}.22,4=2,72\left(l\right)\)

Gọi \(\left\{{}\begin{matrix}n_{CO}=a\left(mol\right)\\n_{CH_4}=b\left(mol\right)\end{matrix}\right.\Rightarrow28a+16b=2,04\left(1\right)\)
\(n_{CaCO_3}=\dfrac{9,6}{100}=0,096\left(mol\right)\)
PTHH: \(2CO+O_2\xrightarrow[]{t^o}2CO_2\)
a------------>a
\(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
b---------------->b
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,096<--0,096
`=> a + b = 0,096 (2)`
`(1), (2) => a = 0,042; b = 0,054`
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,042}{0,042+0,054}.100\%=43,75\%\\\%V_{CH_4}=100\%-43,75\%=56,25\%\end{matrix}\right.\)

5.
\(n_X=\dfrac{2,24}{22,4}=0,1mol\\ M_X=2,125.4=8,5g\cdot mol^{^{ }-1}\\ n_{H_2}=a;n_{C_2H_4}=b\\ a+b=0,1\\ 2a+28b=8,5.0,1=0,85\\ a=0,075;b=0,025\\ H_2+C_2H_4-^{^{ }Ni,t^{^{ }0}}->C_2H_6\\ V_{C_2H_6}=0,025.22,4=0,56L;V_{H_2dư}=22,4\left(0,075-0,025\right)=1,12L\)
6.
Thu được Y chỉ gồm hydrocarbon nên khí hydrogen phản ứng hết.
\(n_A=\dfrac{4,48}{22,4}=0,2mol\\ n_Y=\dfrac{3,36}{22,4}=0,15mol\\ \Delta n_{hh}=n_{H_2\left(pư\right)}=0,05\left(mol\right)\\ n_{C_2H_4}=0,15\left(mol\right)\\ a.\%V_{H_2}=\dfrac{0,05}{0,2}=25\%\\ \%V_{C_2H_4}=75\%\\ b.BTLK\pi:0,15=0,05+n_{Br_2}\\ n_{Br_2}=0,1mol\)

Ta có: \(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo PT: \(n_{CO_2}=n_{CaCO_3}=0,1\left(mol\right)\)
\(n_{hh}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
% số mol cũng là % thể tích.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO_2}=\dfrac{0,1}{0,3}.100\%\approx33,33\%\\\%V_{CO}\approx66,67\%\end{matrix}\right.\)