Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có: nH2SO4 \(=\frac{4,9}{98}=0,05\left(mol\right)\)
Vì: \(x_1+H2S\text{O4}\rightarrow X_2+X_3\) nên X1 có thể là: oxit bazo, oxit lưỡng tính, bazo, hidroxit lưỡng tính, muối. Nhưng vì bài cho X1 có thể là CaO,MgO,NaOH,KOH,Zn và Fe nên loại các trường hợp oxit lưỡng tính, hidroxit lưỡng tính, muối.
TH1: X1 là oxit bazo: CaO,MgO.
Gọi CTPT chung cho X1 là MgO.
PTPU:
MO + H2SO4 → MSO4 + H2O (*) mol
0,05 0,05 0,05
Vậy KL mol của MO là: \(M_{MO}=\frac{2,8}{0,05}=56\left(g\right)\)
Vậy MO là CaO
TH2: Xét X1 là bazo: NaOH, KOH
Gọi CTPT chung cho X1 là MOH.
PTPƯ: 2MOH + H2SO4 → M2SO4 + 2H2SO4 (**)
0,1 0,05 0,05
Vậy KL mol của MOH là: \(M_{MOH}=\frac{2,8}{0,1}=28\left(g\right)\) (không có MOH thỏa mản)
TH3: X1 kim loại Zn và Fe. Gọi CTCP chung cho X1 là M.
PTPU: M + H2SO4 → MSO4 + H2 (***)
0,05 0,05 0,05
Vậy KL mol MO là \(M_M=\frac{2,8}{0,05}=56\left(g\right)\). Vậy M là Fe.
b. X1 là CaO thì X2 là \(m_{CaS\text{O4}}=0,05.136=6,8\left(g\right)\)
(khác bài ra 7,6 g) loại.
X1 là kim loại Fe thì X2 \(m_{FeS\text{O4}}=0,05.152=7,6\left(g\right)\) phù hợp với đề bài như vậy X3 là H2

n Ca OH 2 = 0,02 x 2,5 = 0,05 mol
CO 2 + Ca OH 2 → CaCO 3 + H 2 O
0,05 0,05 0,05 (mol)
Số mol CO 2 dư : 0,075 - 0,05 = 0,025 (mol) nên có phản ứng
CO 2 + CaCO 3 + H 2 O → Ca HCO 3 2
0,025 0,025 0,025 (mol)
Dung dịch thu được có 0,025 mol Ca HCO 3 2
C M Ca HCO 3 2 = 0,025/0,25 = 0,01M





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{7,168}{22,4}=0,32\left(mol\right)\)
Pt : 2Al + 3H2SO4 → Al2(SO4)3 + 3H2\(|\)
2 3 1 3
a 0,32
Mg + H2SO4 → MgSO4 + H2\(|\)
1 1 1 1
b 0,32
Gọi a là số mol của Al
b là số mol của Mg
Theo đề ta có : mAl Mg+ m = 6,6 (g)
⇒ nAl . MAl + nMg . MMg = 6,6 g
27a + 24b = 6,6g (1)
Theo phương trình : 3a + 1b = 0,32 (2)
Từ (1),(2), ta có hệ phương trình :
27a + 24b = 6,6
3a + 1b = 0,32
⇒ \(\left\{{}\begin{matrix}a=0,024\\b=0,248\end{matrix}\right.\)
Khối lượng của nhôm
mAl = nAl . MAl
= 0,024 .27
= 0,648 (g)
Khối lượng của magie
mMg = nMg . MMg
= 0,248 . 24
= 5,952 (g)
Pt : H2 + CuO → (to) Cu + H2O\(|\)
1 1 1 1
0,32 0,32
Số mol của đồng
nCu = \(\dfrac{0,32.1}{1}=0,32\left(mol\right)\)
Khối lượng của đồng
mCu = nCu . MCu
= 0,32 . 64
= 20,48 (mol)
Chúc bạn học tốt

Khối lượng chất rắn giảm đi là khối lượng khí CO 2 bay ra
n CO 2 = 3,3/44 = 0,075 mol
Phương trình hoá học của phản ứng:
CaCO 3 → t ° CaO + CO 2
a mol a mol
XCO 3 → t ° XO + CO 2
2a mol 2a mol
Theo phương trình hoá học trên và dữ kiện đề bài, ta có :
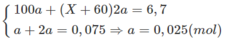
Giải hệ phương trình trên ta thu được : X = 24 (Mg).

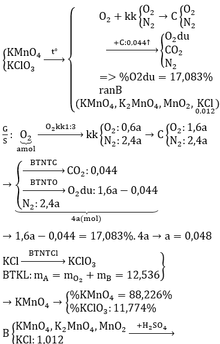

chắc là 4,72g chứ, sao 0,035 mol Ba(OH)2 ra được 4,72kg BaCO3
a)
Gọi \(\left\{{}\begin{matrix}n_{KClO_3}=a\left(mol\right)\\n_{KMnO_4}=2a\left(mol\right)\\n_{CaCO_3}=3a\left(mol\right)\end{matrix}\right.\)
=> mA = 122,5a + 316a + 300a = 738,5a (g)
\(\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{122,5a}{738,5a}.100\%=16,588\%\\\%m_{KMnO_4}=\dfrac{316a}{738,5a}.100\%=42,789\%\\\%m_{CaCO_3}=\dfrac{300a}{738,5a}.100\%=40,623\%\end{matrix}\right.\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
a------------>a---->1,5a
2KMnO4 --to--> K2MnO4 + MnO2 + O2
2a-------------->a---------->a------->a
CaCO3 --to--> CaO + CO2
3a----------->3a---->3a
B chứa\(\left\{{}\begin{matrix}KCl:a\left(mol\right)\\K_2MnO_4:a\left(mol\right)\\MnO_2:a\left(mol\right)\\CaO:3a\left(mol\right)\end{matrix}\right.\)
=> mB = 74,5a + 197a + 87a + 168a = 526,5a (g)
=> \(\left\{{}\begin{matrix}\%m_{KCl}=\dfrac{74,5a}{526,5a}.100\%=14,15\%\\\%m_{K_2MnO_4}=\dfrac{197a}{526,5a}.100\%=37,417\%\\\%m_{MnO_2}=\dfrac{87a}{526,5a}.100\%=16,524\%\\\%m_{CaO}=\dfrac{168a}{526,5a}.100\%=31,909\%\%\end{matrix}\right.\)
b)
khí C chứa \(\left\{{}\begin{matrix}O_2:2,5a\left(mol\right)\\CO_2:3a\left(mol\right)\end{matrix}\right.\)
\(n_{Ba\left(OH\right)_2}=0,5.0,07=0,035\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{4,72}{197}\approx0,024\left(mol\right)\)
TH1: Nễu kết tủa không bị hòa tan
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,024<--0,024
=> 3a = 0,024
=> a = 0,008
V = (2,5a + 3a).22,4 = 0,9856 (l)
mA = 738,5a = 5,908 (g)
TH2: Nếu kết tủa bị hòa tan 1 phần
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,035--->0,035--->0,035
BaCO3 + CO2 + H2O --> Ba(HCO3)2
0,011--->0,011
=> 3a = 0,035 + 0,011
=> a = \(\dfrac{23}{1500}\)
=> V = (2,5a + 3a).22,4 = 1,889 (l)
mA = 738,5a = 11,3237 (g)