Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nHCl=\(\dfrac{100,85.1,19.36,5\%}{36,5}\)=1,19(mol)
Bảo toàn nguyên tố Cl => nCuCl2=\(\dfrac{1}{2}n_{HCl}\) =0,595(mol)
Ta có : nCu(OH)2=0,4(mol)=nCuCl2n <0,595
=> HCl dư khi tác dụng với hỗn hợp A
CuO+2HCl−−−>CuCl2+H2O
0,4<----0,8<-------0,4
=> Chất rắn C không tan chỉ có Cu
nSO2=\(\dfrac{11,2}{22,4}\)=0,5(mol)
Cu+2H2SO4(đ,n)−−−>CuSO4+SO2↑+2H2O
0,5<-------------------------------------0,5
=>
\(\%m_{CuO}=\dfrac{0,4.80}{0,4.80+0,5.64}.100=50\%\)
=>%mCu =100-50=50%
b, 2NaOH+CuCl2−−−>2NaCl+Cu(OH)2↓
0,8<----------0,4<-----------------------0,4
=> \(m_{ddNaOH}=\dfrac{0,8.40}{25\%}=128\left(g\right)\)
=> VddNaOH=\(\dfrac{128}{1,28}\)=100(ml)

Gọi x, y lần lượt là số mol của CuO và Cu
nHCl=100*1,19*36,5/100*36,5=1,19(mol)=> nCuCl2=0,595(mol)
nCu(OH)2=0,4(mol)=nCuCl2<0,595
=> HCl dư khi tác dụng với hỗn hợp ban đầu
CuO+2HCl−−−>CuCl2+H2O
....0,4........0,8........0,4..............
=> Chất rắn B không tan chính là Cu
nSO2=0,5(mol)
Cu+2H2SO4(đ,n)−−−>CuSO4+SO2↑+2H2O
0,5..............................................................0,5..............
=>
%CuO=50%
%Cu=50%
b,
2NaOH+CuCl2−−−>2NaCl+Cu(OH)2↓
.....0,8.........0,4...................................................0,4..........................
=> mNaOH=32(g)
=> mddNaOH=128(g)
=> VddNaOH=100(ml)=V
@lâm khánh đại mình nhầm chỗ kia là 1,2 mà mình quen dùng 1,19 á nên nhầm
m dung dịch HCl = 100*1,2 = 120g
m HCl trong dung dịch = 120* 36,5 / 100 = 43.8 g
=> nHCl = 43,8/ 36,5 = 1.2 mol
bạn đặt lại lên phương trình rồi tính lại giúp mình nhé

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
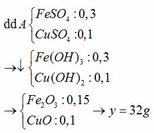

Cho hỗn hợp X vào dung dịch HCl lấy dư:
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Fe + 2HCl → FeCl2 + H2
Dung dịch Y gồm: AlCl3, MgCl2, FeCl2, HCl dư
Khí Z là H2
Chất rắn A là Cu
Cho A tác dụng với H2SO4 đặc nóng.
PTHH: Cu + 2H2SO4(đặc, nóng) → CuSO4 + SO2 + 2H2O
Khí B là SO2
Cho B vào nước vôi trong lấy dư
PTHH: SO2 + Ca(OH)2 → CaSO3 + H2O
Kết tủa D là CaSO3
Cho dung dịch NaOH vào Y tới khi kết tủa lớn nhất thì dừng lại.
PTHH: NaOH + HCl → NaCl + H2O
3NaOH + AlCl3 → Al(OH)3 + 3NaCl
2NaOH + MgCl2 → Mg(OH)2 + 2NaCl
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Chất rắn E là: Al(OH)3, Mg(OH)2, Fe(OH)2
Nung E trong không khí
Chất rắn G là Al2O3, MgO, Fe2O3

nH2 = 0,13 mol; nSO2 = 0,25 mol
Ta có
2H+ + 2e → H2 Cu → Cu2+ + 2e
0,26 ←0,13 0,12 0,24
S+6 + 2e → S+4
0,5 ← 0,25
TH1: M là kim loại có hóa trị không đổi
=> nCu = (0,5 – 0,26) : 2 = 0,12 mol => mCu = 7,68g
=> mM = 3,12g (loại vì khối lượng của M lớn hơn của Cu)
TH2: M là kim loại có hóa trị thay đổi
Do M không có hóa trị I do đó khi phản ứng với HCl thì M thể hiện hóa trị II
M + 2HCl → MCl2 + H2
0,13 ← 0,13
Do M có hóa trị thay đổi => khi phản ứng với H2SO4 đặc nóng thì M thể hiện hóa trị III
2M + 6H2SO4 → M2(SO4)3 + 3SO2 + 6H2O
0,13 → 0,195
Cu + 2H2SO4 → CuSO4+ SO2 + 2H2O
0,055 ← 0,055
=> mM = 10,8 – 0,055 . 64 = 7,28g
=> MM = 56 => Fe
Ta có số mol của Cu và Fe trong 10,8 g lần lượt là 0,055 và 0,13 mol
=> Trong 5,4g có số mol Cu và Fe lần lượt là 0,0275 và 0,065 mol
nAgNO3 = 0,16mol
Fe + 2AgNO3 → Fe(NO3)2 +2Ag
0,065 0,13 0,065 0,13
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
0,015 0,03 0,03
=> nCu dư = 0,0275 – 0,015 = 0,0125mol
m = mCu dư + mAg = 0,0125 . 64 + 0,16 . 108 = 18,08g

Nung hỗn hợp BaCO3, Cu, FeO chỉ có BaCO3 bị nhiệt phân hủy
BaCO3 → t ∘ BaO + CO2↑ (B)
Rắn A gồm: Cu, FeO, BaO, có thể có BaCO3 dư
Khí B là CO2
CO2 + KOH → KHCO3
CO2 + 2KOH → K2CO3 + H2O
Dung dịch C gồm KHCO3 và K2CO3
KHCO3 + NaOH → K2CO3 + Na2CO3 + H2O
K2CO3 + CaCl2 → CaCO3↓ + 2KCl
A + H2O dư có phản ứng xảy ra:
BaO + H2O → Ba(OH)2
Vây dd D là Ba(OH)2
rắn E là Cu, FeO, có thể có BaCO3 dư
E + HCl dư → khí B + dd F + rắn G
BaCO3 + 2HCl → BaCl2 + CO2↑ + H2O
FeO + 2HCl → FeCl2 + H2O
Dd F gồm: BaCl2, FeCl2 và HCl dư
Rắn G là Cu
A + H2SO4 đặc => hỗn hợp khí H ( từ đây khẳng định chắc chắn A có BaCO3 dư)
BaCO3 + H2SO4 đặc → t ∘ BaSO4↓ + CO2 + H2O
Cu + 2H2SO4 đặc → t ∘ CuSO4 + SO2↑ + 2H2O
2FeO + 4H2SO4 đặc → t ∘ Fe2(SO4)3 + SO2 + 4H2O
Hỗn hợp khí H gồm: SO2 và CO2
Dung dịch I gồm: CuSO4, Fe2(SO4)3, H2SO4 đặc, nóng dư
Kết tủa K là: BaSO4.







CuO +2HCl --> CuCl2 +H2O (1)
Cu +2H2SO4 -to-> CuSO4 +SO2 +2H2O (2)
CuCl2 +2NaOH --> Cu(OH)2 +2NaCl (3)
mdd HCl=120,0115(g)
=>nHCl=1,2(mol)
nCu(OH)2=0,4(mol)
nSO2=0,5(mol)
theo(3) : nCuCl2=nCu(OH)2=0,4(mol)
theo(1) :nCuO=nCuCl2=0,4(mol)
=>mCuO=32(g)
theo(2) : nCu=nSO2=0,5(mol)
=>mCu=32(g)
=>%mCu=50(%)
%mCuO=50(%)
b)theo(3) : nNaOH=2nCu(OH)2=0,8(mol)
=>mNaOH=32(g)
=>mdd NaOH=128(g)
=>V=128/1,28=100(ml)