
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

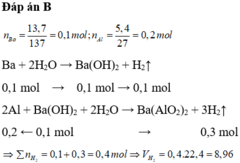

a)
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$n_{H_2} = \dfrac{13,44}{22,4} = 0,6(mol)$
Theo PTHH :
$n_{Al} = \dfrac{2}{3}n_{H_2} = 0,4(mol)$
$m_{Al} = 0,4.27 = 10,8(gam)$
$m_{Cu} = 20,4 - 10,8 = 9,6(gam)$
b) $n_{H_2SO_4} = n_{H_2} = 0,6(mol)$
$m = \dfrac{0,6.98}{14,7\%} = 400(gam)$

\(n_{Ba\left(OH\right)_2}=\dfrac{20.52}{171}=0.12\left(mol\right)\)
\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(n_{NaOH}=a\left(mol\right)\)
\(n_H=0.12\cdot2+a+0.05\cdot2=0.34+a\left(mol\right)\)
\(\Rightarrow n_{H_2O}=0.17+0.5a\left(mol\right)\)
\(BTKL:\)
\(21.9+\left(0.17+0.5a\right)\cdot18=20.52+40a+0.05\cdot2\)
\(\Rightarrow a=0.14\)
\(m_{NaOH}=0.14\cdot40=5.6\left(g\right)\)
Quy đôi A gồm : Na,Ba và O
n Ba = n Ba(OH)2 = 20,52/171 = 0,12(mol)
Gọi n Na = a(mol) ; n O = b(mol)
=> 23a + 16b + 0,12.137 = 21,9(1)
n H2 = 1,12/22,4 = 0,05(mol)
Bảo toàn e :
$Na^0 \to Na^+ + 1e$
$Ba^0 \to Ba^{+2} + 2e$
$O^0 + 2e \to O^{-2}$
$2H^+ 2e \to H_2$
=> a + 0,12.2 = 2b + 0,05.2(2)
Từ (1)(2) suy ra a = b = 0,14
n NaOH = n Na = 0,14 mol
=> m NaOH = 0,14.40 = 5,6(gam)

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


a. Phương trình phản ứng :
C2H2 + 2Br2 → C2H2Br4 (1)
C2H4 + Br2 → C2H4Br2 (2)
b. Hỗn hợp khí B gồm có H2, C2H6. Gọi x, y ( mol ) lần lượt là số mol của H2 và C2H6 có trong 6,72 lít hỗn hợp B.
nB = x + y = 6,72 : 22,4 = 0,3 mol (I)
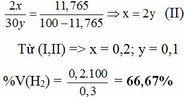
% V(C2H6) = 100% – 66,67% = 33,33%
c. nA = 11,2 : 22,4 = 0,5 mol , M A = 0,4 . 44 = 17,6 g/ mol
mA = 0,5 . 17,6 = 8,8 gam
mB = 0,2 . 2 + 0,1 . 30 = 3,4 gam
Vậy khối lượng bình Br2 tăng: m = mA – mB = 8,8 – 3,4 = 5,4 gam.

Đáp án B
Phần chất rắn chưa tan là Al còn dư
Gọi n K = x mol
Cho hỗn hợp X vào nước, K phản ứng hết tạo KOH và Al phản ứng với KOH và còn dư => tính số mol theo KOH
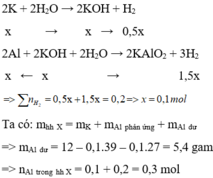
Cho hỗn hợp X tác dụng với dung dịch KOH dư => K phản ứng hết với H 2 O và Al phản ứng hết với KOH
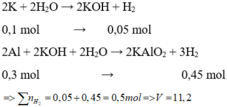

Coi V = 22,4(lít)
Thí nghiệm 1 : $Al$ dư
$n_{H_2} = 1(mol)$
Gọi $n_{Na} = a(mol)$
$2Na + 2H_2O \to 2NaOH + H_2$
$2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
Theo PTHH :
$n_{H_2} = 0,5a + 1,5a = 1 \Rightarrow a = 0,5(mol)$
Thí nghiệm 2 : $Al$ hết
Gọi $n_{Al} = b(mol)$
Theo PTHH :
$n_{H_2} = \dfrac{1}{2}n_{Na} + \dfrac{3}{2}n_{Al}$
$\Rightarrow \dfrac{1}{2}.0,5 + \dfrac{3}{2}b = 1,75$
$\Rightarrow b = 1(mol)$
Ta có :
$\%m_{Na} = \dfrac{0,5.23}{0,5.23 + 1.27}.100\% = 29,87\%$
Đáp án D

\(V_{C_2H_6}=13,44-6,72=6,72\left(l\right)\)
=> \(n_{C_2H_6}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{C_2Ag_2}=\dfrac{24}{240}=0,1\left(mol\right)\)
=> \(n_{C_2H_2}=0,1\left(mol\right)\)
=> \(n_{C_2H_4}=\dfrac{13,44}{22,4}-0,3-0,1=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}\%m_{C_2H_6}=\dfrac{0,3.30}{0,3.30+0,2.28+0,1.26}.100\%=52,326\%\\\%m_{C_2H_4}=\dfrac{0,2.28}{0,3.30+0,2.28+0,1.26}.100\%=32,558\%\\\%m_{C_2H_2}=\dfrac{0,1.26}{0,3.30+0,2.28+0,1.26}.100\%=15,116\%\end{matrix}\right.\)

Gọi số mol của Ba, Al và Mg lần lượt là x, y và z mol
Lượng khí thu được khi cho A vào nước dư ít hơn khi cho A vào xút dư nên khi cho A vào nước dư thì Ba phản ứng hết, Al phản ứng một phần. Khi cho A vào xút dư thì cả Ba và Al đều phản ứng hết.
Cho A tác dụng với nước dư có phản ứng:
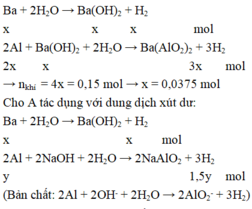

Khối lượng của A là: m = 0,0375.137 + 0,175.27 + 0,1.24 = 12,2625 gam.
⇒ Chọn B

Có thiếu đề không bạn ? Nếu không cho kim loại cụ thể bài này không làm được!