Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sửa đề dung dịch axit clohidric phải là HCl chứ nhỉ
\(n_{H2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2<----0,6<-------------------0,3
\(a=m_{Al}=0,2.27=5,4\left(g\right)\)
\(x=C_{MddHCl}=\dfrac{0,6}{0,2}=3\left(M\right)\)

Số mol của khí hidro ở dktc
nH2 =\(\dfrac{V_{H2}}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : X + 2HCl → XCl2 + H2\(|\)
1 2 1 1
0,1 0,1
Số mol của kim loại X
nX = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ MX = \(\dfrac{m_X}{n_X}=\dfrac{5,6}{0,1}=56\) (dvc)
Vậy kim loại x là Fe
⇒ Chọn câu : B Chúc bạn học tốt
\(R+2HCl \rightarrow RCl_2+H_2\\ n_{H_2}=\frac{2,24}{22,4}=0,1mol\\ M_R=\frac{5,6}{0,1}=56 g/mol\\ \Rightarrow R: Fe\)

Tham khảo
Gọi số mol của Fe và Al trong hỗn hợp lần lượt là x và y (x,y∈N*)(x,y∈N*)
Số mol H2 thu được là: nH2=8,9622,4=0,4(mol)nH2=8,9622,4=0,4(mol)
PTHH:
Fe+2HCl→FeCl2+H2↑(1)2Al+3HCl→2AlCl3+3H2(2)Fe+2HCl→FeCl2+H2↑(1)2Al+3HCl→2AlCl3+3H2(2)
Theo PTHH (1): nFe=x⇒nH2=xnFe=x⇒nH2=x
Theo PTHH (2): nAl=y⇒nH2=32ynAl=y⇒nH2=32y
Từ các PTHH và đề bài ta có:
(I)⎧⎨⎩x+32y=0,456x+27y=11(I){x+32y=0,456x+27y=11
Giải hệ phương trình I ta được x = 0,1 ; y = 0,2
Khối lượng của Fe và Al trong hỗn hợp là:
mFe=0,1.56=5,6(g)mAl=0,2.27=5,4(g)mFe=0,1.56=5,6(g)mAl=0,2.27=5,4(g)
Thành phần phần trăm khối lượng Fe và Al trong hỗn hợp là:
%mFe=5,611⋅100≈50,91%%mAl=100%−50,91%=49,09%%mFe=5,611⋅100≈50,91%%mAl=100%−50,91%=49,09%
b) Từ PTHH (1) ta có: nHCl(1)=2x=0,2(mol)nHCl(1)=2x=0,2(mol)
Từ PTHH (2) ta có: nHCl(2)=3y=0,6(mol)nHCl(2)=3y=0,6(mol)
Tổng số mol HCl tham gia phản ứng với hỗn hợp là:
nHCl=0,2+0,6=0,8(mol)nHCl=0,2+0,6=0,8(mol)
Thể tích dung dịch HCl 2M cần dùng:
VHCl(2M)=0,82=0,4(l)VHCl(2M)=0,82=0,4(l)
c) 0,4l = 400ml
Khối lượng dung dịch HCl 2M cần dùng là:
mHCl(2M)=VHCl(2M).DHCl(2M)=400.1,12=448(g)mHCl(2M)=VHCl(2M).DHCl(2M)=400.1,12=448(g)
Dung dịch thu được sau phản ứng có chứa muối FeCl2 và AlCl3
Khối lượng của dung dịch sau phản ứng là:
mdd=mhh+mHCl−mH2=11+488−0,8=458,2(g)mdd=mhh+mHCl−mH2=11+488−0,8=458,2(g)
theo PTHH nFeCl2=nFe=0,1(mol)nAlCl3=nAl=0,2(mol)nFeCl2=nFe=0,1(mol)nAlCl3=nAl=0,2(mol)
Khối lượng FeCl2 và AlCl3 thu được là:
mFeCl2=0,1.127=12,7(g)mAlCl3=0,2.133,5=26,7(g)mFeCl2=0,1.127=12,7(g)mAlCl3=0,2.133,5=26,7(g)
Nồng độ phần trăm các dung dịch thu được là:
C%FeCl2=12,7458,2⋅100≈2,77%

Có V1 < V2 => khi X tác dụng với H2O thì Al còn dư.
Giả sử số mol 3 kim loại là: x, y, z.
K + H2O → KOH + ½ H2↑
x → x 0,5x
Al + KOH + H2O → KAlO2 + 1,5H2↑
x ← x→ 1,5x
→ 0,5x + 1,5x = 0,2 → x = 0,1
X tác dụng với KOH: 0,1 . 0,5 + 1,5y = 0,35 => y = 0,2
Khi cho X tác dụng với H2O còn dư Al => Y chứa Al dư và Fe
nAl dư = nAl ban đầu – nAl phản ứng = 0,2 – 0,1 = 0,1mol
=> 0,1 . 1,5 + z = 0,4 => z = 0,25mol
=> m = 23,3g

-Đặt số mol của Mg và kim loại M lần lượt là : x và y
Các phương trình hóa học:
Mg + 2HCl → MgCl2 + H2
x................................................x
2M + 2nHCl → 2MCln + nH2 (có thể có)
y...................................................\(\dfrac{ny}{2}\)
Mg + 2H2SO4 → MgSO4 + SO2 + 2H2O
x....................................................x
2M + 2mH2SO4 → M2(SO4)m + mSO2 + 2mH2O
y ..........................................................\(\dfrac{my}{2}\) ![]()
Số mol của H2 là : \(\dfrac{8,96}{22,4}\) = 0,4 mol
Số mol của SO2 là : \(\dfrac{11,2}{22,4}\) = 0,5 mol
Trường hợp 1. Kim loại M không phản ứng với dung dịch HCl.
Theo bài ra và các phương trình trên ta có :
24x + My = 16 (1)
x = 0,4 (2)
x + \(\dfrac{my}{2}\)= 0,5 (3)
Từ (1), (2), (3) ta có : M = 32m
-Nếu m = 1 → M = 32 (loại)
-Nếu m = 2 → M = 64 (Cu)
-Nếu m = 3 → M = 96 (loại)
\(\rightarrow\)Vậy kim loại M là Cu
- Trường hợp 2. Kim loại M phản ứng với dung dịch HCl.
Theo bài ra và các phương trình trên ta có :
24x + My = 16 (4)
x +\(\dfrac{ny}{2}\) = 0,4 (5)
x + \(\dfrac{my}{2}\)= 0,5 (6)
Theo (5) và (6) thấy m > n
|
n |
1 | 1 | 2 |
|
m |
2 |
3 |
3 |
|
x |
0,3 |
0,35 |
0,2 |
|
y |
0,2 |
0,1 |
0,2 |
|
M |
44 (loại) |
76 (loại) |
56 (Fe) |
Vậy kim loại M là Fe

\(a/\\3Al+2H_2SO_4 \to Al_2(SO_4)_3+3H_2\\ Zn+H_2SO_4 \to ZnSO_4+H_2\\ n_{H_2SO_4}=\frac{400.9.8\%}{98}=0,4(mol)\\ n_{Al}=a(mol)\\ n_{Zn}=b(mol) m_{hh}=27a+65b=11,9(1)\\ n_{H_2SO_4}=1,5a+b=0,4(mol)\\ (1)(2)\\ a=0,2; b=0,1\\ b/\\ \%m_{Al}=\frac{0,2.27}{11,9}.100=45,38\%\\ \%m_{Zn}=54,62\% \)

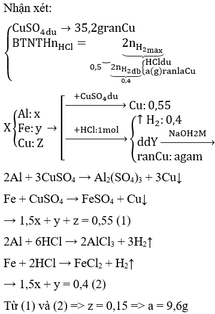

\(n_{H2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(n_{H2}=n_{H2SO4}=0,4\left(mol\right)\)
\(\Rightarrow C\%_{ddH2SO4}=\dfrac{0,4.98}{200}.100\%=19,6\%\)