Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : A
Y làm mất màu n K M N O 4 = 10.0,03.0,2 = 0,06 mol
=> n F e 2 + = 5 n K M N O 4 (bảo toàn e) = 0,3 mol
Xét m gam X có : 0,258m (g) O
=> n F e 3 O 4 = 4,03125.10-3m (mol) > nCu = 1,012.10-3m (mol)
=> Cu hết
Fe3O4 -> Fe2+ + 2Fe3+
2Fe3+ + Cu -> 2Fe2+ + Cu2+
=> n F e 2 + s a u = 6,055.10-3m (mol) = 0,3 mol
=> m = 49,55g

Thứ tự xảy ra các phản ứng là:
Fe₃O₄ + H₂SO₄ → FeSO₄ + Fe₂(SO₄)₃ + 4H₂O
Cu + Fe₂(SO₄)₃ → CuSO₄ + 2FeSO₄ (*)
10FeSO₄ + 8H₂SO₄ + 2KMnO₄ → 5Fe₂(SO₄)₃ + K₂SO₄ + 2MnSO₄ + 8H₂O
→ nFeSO₄ = 5nKMnO₄ = 0,245 mol; nCu = m ÷ 64 mol; nFe₃O₄ = 5m ÷ 232
→ nFe₂(SO₄)₃ = 5m ÷ 232 > nCu → Fe₂(SO₄)₃ dư ở phản ứng (*)→ nFeSO₄ (*) = nCu = m ÷ 64 mol
→ ∑nFeSO₄ = 5m ÷ 232 + 2 × m ÷ 64 = 0,245 mol → m = 4,64(g) → Đáp án D

Đáp án : D
nH+ = nHCl + 2nH2SO4 = 0,1 mol
Dung dịch sau có pH = 13 => COH- = 0,1M => nOH- = 0,04 mol
=> nOH (Y) = 0,14 mol = ånKL.(số điện tích)
Lại có : 2nH2 = nOH ( do các kim loại tạo ra) = 0,14 mol với 400 ml Y
=> Với 200 ml dung dịch Y có nOH tạo ra do kim loại = 0,07 mol
=> nOH tạo ra do oxit = 0,07 mol = ånKL(oxit).(số điện tích) = 2nO (bảo toàn điện tích)
=> nO = 0,035 mol
Để tạo 400 ml Y thì nO = 0,035.2 = 0,07 mol
=> m = 12,8g

Chọn B.
Dung dịch sau có pH = 13 nên sau phản ứng còn dư kiềm: nOH-dư = 0,1.0,4 = 0,04 mol.
⇒ n O H - Y = 0,04+0,2.(0,2+0,2.0,15)=0,14 mol
Quy đổi X tương đương với hỗn hợp gồm: Na (x mol), K (y mol), Ba (z mol), O (t mol).
⇒ l6t = 8,75% m.
Theo định luật bảo toàn electron, ta có: x + y + z = 2t + 2 n H 2
⇒ t = (2.0,14 - 2.0,07) : 2 = 0,07 mol ⇒ m = 12,8 ≈ 13 gam.

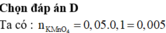
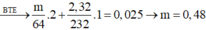
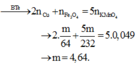



Chọn A.