Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\\n_{H_2SO_4}=0,4\cdot1=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{ZnSO_4}=0,3\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{ZnSO_4}}=\dfrac{0,3}{0,4}=0,75\left(M\right)\\C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,1}{0,4}=0,25\left(M\right)\end{matrix}\right.\)

Chọn D
Gọi số mol của FeO và CuO lần lượt là x và y mol
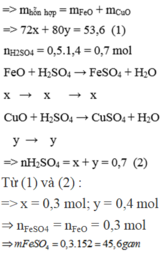
Ta có: m d d H 2 S O 4 = D . V = 1 , 2 . 500 = 600 g a m
Vì phản ứng không tạo ra chất khí hay kết tủa nên:
m d d s a u p ư = m t r ư ớ c p ư = m h h A + m d d a x i t = 53 , 6 + 600 = 653 , 6 g a m .
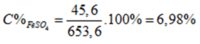

\(n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,15 0 ,05 0,15
a)\(V=0,15\cdot22,4=3,36\left(l\right)\)
b)\(m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,7}{9,8}\cdot100=150\left(g\right)\)
c) \(m_{H_2}=0,15\cdot2=0,3\left(g\right)\)
\(m_{ddsau}=2,7+150-0,3=152,4\left(g\right)\)
\(m_{Al_2\left(SO_4\right)_3}=0,05\cdot342=17,1\left(g\right)\)
\(\Rightarrow C\%=\dfrac{17,1}{152,4}\cdot100=11,22\%\)

nCuSO4 =16/160 = 0,1(mol) ; nNaOH = 12/40 = 0,3 (mol)
a) PTHH
CuSO4 + 2NaOH -------> Cu(OH)2 + Na2SO4
b)
PTHH:
_________CuSO4 + 2NaOH -------> Cu(OH)2 + Na2SO4
ban đầu: 0,1-------->0,3
phản ứng: 0,1-------->0,2------------->0,1--------...
kết thúc: 0----------->0,1--------------->0,1_____...
Sau phản ứng khối lượng chất rắn thu được là:
mCu(OH)2 = 0,1*98 = 9,8 (g)
c)
Khi cho 40ml dung dịch có chứa 16g CuSO4 với 60 ml dung dịch có chứa 12g NaOH thì thể tích sau khi pản ứng là:
V = 60 + 40 = 100 (ml) = 1 (l)
Sau phản ứng thu được:
0,1 mol Na2SO4 và 0,1 mol NaOH (dư)
Vậy nồng độ của Na2SO4 và NaOH sau phản ứng lần lượt là
CM(Na2SO4) = n/V = 0,1/0,1=1 (M)
CM(NaOH) = n/V = 0,1/0,1 = 1 (M).
cho 8g fe2o3 phản ứng hoàn toàn với dung dịch HCl 1M . Viết phương trình hóa hôc của phản ứng trên . Tính thể tích dung dịch HCl 1M cần dùng .Tính nồng độ phần trăm của chất có trong dung dịch sau phản ứng biết rằng thể tích thay đổi không đáng kể
Gỉai dùm bài này đi ạ e thi mà e ko biết đúng

\(a.n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\\ a.CuO+2HCl\rightarrow CuCl_2+H_2O\\ 0,05.......0,1........0,05.......0,05\left(mol\right)\\ b.m_{CuCl_2}=135.0,05=6,75\left(g\right)\\ b.C_{MddHCl}=\dfrac{0,1}{0,1}=1\left(M\right)\)
Câu 3 :
\(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\)
a) Pt : \(CuO+2HCl\rightarrow CuCl_2+H_2O|\)
1 2 1 1
0,05 0,1 0,05
b) \(n_{CuCl2}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
⇒ \(m_{CuCl2}=0,05.135=6,75\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,05.2}{1}=0,1\left(mol\right)\)
100ml = 0,1l
\(C_{M_{ddHCl}}=\dfrac{0,1}{0,1}=1\left(M\right)\)
Chúc bạn học tốt

a) $Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O$
b) $n_{Al_2O_3} = \dfrac{15,3}{102} = 0,15(mol)$
$\Rightarrow n_{AlCl_3} =0,15.2 = 0,3(mol)$
$m_{AlCl_3} =0,3.133,5 = 40,05(gam)$
c) $n_{HCl}= 6n_{Al_2O_3} = 0,9(mol)$
$C_{M_{HCl}} = \dfrac{0,9}{0,3} = 3M$
Số mol của nhôm oxit
nAl2O3= \(\dfrac{m_{Al2O3}}{M_{Al2O3}}=\dfrac{15,3}{102}=0,15\left(mol\right)\)
a) Pt : Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O\(|\)
1 3 1 3
0,15 0,45 0,15
b) Số mol của muối nhôm sunfat
nAl2(SO4)3 = \(\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
Khối lượng của muối nhôm sunfat
mAl2(SO4)3 = nAl2(SO4)3 . MAl2(SO4)3
= 0,15 . 342
= 51,3 (g)
c) Số mol của axit sunfuric
nH2SO4 = \(\dfrac{0,15.3}{1}=0,45\left(mol\right)\)
300ml = 0,3l
Nồng độ mol của axit sunfuric đã phản ứng
CMH2SO4 = \(\dfrac{n}{V}=\dfrac{0,45}{0,3}=1,5\left(M\right)\)
Chúc bạn học tốt

a, Hiện tượng: có kết tủa trắng.
\(n_{KCl}=0,4\cdot2=0,8\left(mol\right);n_{AgNO_3}=2\cdot0,1=0,2\left(mol\right)\\ PTHH:KCl+AgNO_3\rightarrow KNO_3+AgCl\downarrow\\ ....0,2....0,2.....0,2....0,2\left(mol\right)\)
Vì \(\dfrac{n_{KCl}}{1}>\dfrac{n_{AgNO_3}}{1}\) nên sau phản ứng KCl dư, tính theo AgNO3
\(\Rightarrow m_{AgCl}=0,2\cdot143,5=28,7\left(g\right)\)
\(b,V_{dd\left(sau.p/ứ\right)}=V_{KNO_3}=V_{KCl}+V_{AgNO_3}=0,4+0,1=0,5\left(l\right)\\ \Rightarrow C_{M_{KNO_3}}=\dfrac{0,2}{0,5}=0,4M\)


a) PTHH: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
Hiện tượng: Chất bột tan dần, dd chuyển màu xanh
b+c) Ta có: \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,4\left(mol\right)\\n_{CuCl_2}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{ddHCl}=\dfrac{0,4}{2}=0,2\left(l\right)\\C_{M_{CuCl_2}}=\dfrac{0,2}{0,2}=1\left(M\right)\end{matrix}\right.\)
Số mol của đồng (II) oxit
nCuO = \(\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{16}{80}=0,2\left(mol\right)\)
a) Pt : CuO + H2SO4 → CuSO4 + H2O\(|\)
1 1 1 1
0,2 0,2 0,2
Hiện tượng quan sát được : CuO bị hòa tan trong dung dịch H2SO4 tạo ra dung dịch có màu xanh lam
b) Số mol của dung dịch axit sunfuric
nH2SO4 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Thể tích của dung dịch axit sunfuric cần dùng
CMH2SO4 = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}=\dfrac{0,2}{2}=0,1\left(l\right)\)
c) Số mol cuả muối đồng (II) sunfat
nCuSO4 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Nồng độ mol của của muối đồng (II) sunfat
CM = \(\dfrac{n}{V}=\dfrac{0,2}{0,1}=2\left(M\right)\)
Chúc bạn học tốt