Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sửa đề cho dễ làm: "200g dd HCl 3,65%"
Ta có: \(n_{Na_2CO_3.10H_2O}=\dfrac{14,3}{106+10\cdot18}=0,05\left(mol\right)\) \(\Rightarrow n_{Na_2CO_3}=0,05\left(mol\right)\)
PTHH: \(Na_2CO_3+2HCl\rightarrow2NaCl+H_2O+CO_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Na_2CO_3}=0,05\left(mol\right)\\n_{HCl}=\dfrac{200\cdot3,65\%}{36,5}=0,2\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,2}{2}\) \(\Rightarrow\) Na2CO3 p/ứ hết, HCl còn dư
\(\Rightarrow n_{NaCl}=0,1\left(mol\right)=n_{HCl\left(dư\right)}\) \(\Rightarrow\left\{{}\begin{matrix}m_{NaCl}=0,1\cdot58,5=5,85\left(g\right)\\m_{HCl\left(dư\right)}=0,1\cdot36,5=3,65\left(g\right)\end{matrix}\right.\)
Mặt khác: \(n_{CO_2}=0,05\left(mol\right)\) \(\Rightarrow m_{CO_2}=0,05\cdot44=2,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_{Na_2CO_3.10H_2O}+m_{ddHCl}-m_{CO_2}=212,1\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{NaCl}=\dfrac{5,85}{212,1}\cdot100\%\approx2,76\%\\C\%_{HCl\left(dư\right)}=\dfrac{3,65}{212,1}\cdot100\%\approx1,72\%\end{matrix}\right.\)

\(n_{Na_2CO_3.10H_2O}=\dfrac{28,6}{286}=0,1\left(mol\right)\)
=> nNa2CO3 = 0,1(mol)
=> \(C_M=\dfrac{0,1}{0,2}=0,5M\)
mdd sau pư = 1,05.200 = 210 (g)
=> \(C\%=\dfrac{0,1.106}{210}.100\%=5,05\%\)

$n_{Na_2CO_3} = n_{Na_2CO_3.10H_2O} = \dfrac{28,6}{286} = 0,1(mol)$
$C_{M_{Na_2CO_3}} = \dfrac{0,1}{0,2} = 0,5M$
$m_{dd} = D.V = 200.1,05 = 210(gam)$
$C\%_{Na_2CO_3} = \dfrac{0,1.106}{210}.100\% = 5,05\%$

\(n_{C_2H_5OH}=\dfrac{92}{46}=2\left(mol\right)\)
\(CM_{C_2H_5OH}=\dfrac{2}{0,25}=8M\)
\(C\%_{doruou}=\dfrac{92}{250.0,8}.100=46^o\)

Giải thích các bước giải:
a Để tính nồng độ % của dung dịch CuSO4 bão hòa ở nhiệt độ trên, ta dùng công thức:
Nồng độ % = (Khối lượng chất tan/Công thức phân tử chất tan) / Thể tích dung dịch x 100%
Với dung dịch CuSO4 bão hòa ở 60 độ C, ta có:
Khối lượng chất tan (CuSO4) = 40 kg = 40000 g
Thể tích dung dịch = 100 ml = 100 cm^3
Công thức phân tử CuSO4: 1 Cu + 1 S + 4 O = 63.5 + 32 + 4 x 16 = 159.5
Nồng độ % = (40000/159.5) / 100 = 25.08 %
Vậy, nồng độ % của dung dịch CuSO4 bão hòa ở nhiệt độ 60 độ C là khoảng 25.08 %.
b) Để tính khối lượng H2O cần dùng để pha vào dung dịch trên và có được dung dịch CuSO4 10%, ta dùng công thức:
Khối lượng H2O = Khối lượng chất tan ban đầu - Khối lượng chất tan sau pha / (Nồng độ sau pha - Nồng độ ban đầu)
Giả sử khối lượng chất tan sau khi pha là x g (= 10/100 x khối lượng dung dịch sau khi pha)
Vậy, ta có:
Khối lượng chất tan sau pha = 32 g + x g
Nồng độ sau pha = 10%
Nồng độ ban đầu = 25.08 %
Ứng dụng công thức, ta có:
x = (32 - 0.1 x (32 + x)) / (0.100 - 0.2508)
10000 x = 32 - 0.1 x (32 + x)
10000 x = 32 - 3.2 - 0.1x^2
0.1x^2 - 9967.2x + 3.2 = 0
Giải phương trình trên bằng phương pháp giải phương trình bậc hai ta có:
x ≈ 0.3145 hoặc x ≈ 9965.88
Với x ≈ 0.3145, ta được khối lượng H2O ≈ 32 - 0.3145 = 31.6855 g
Vậy, để có được dung dịch CuSO4 10%, ta cần dùng khoảng 31.6855 g nước.

\(n_{Na_2CO_3}=\dfrac{21,2}{106}=0,2\left(mol\right)\)
=> \(C_M=\dfrac{0,2}{0,3}=0,667M\)
\(m_{dd}=300.1,05=315\left(g\right)\)
=> \(C\%=\dfrac{21,2}{315}.100\%=6,73\%\)

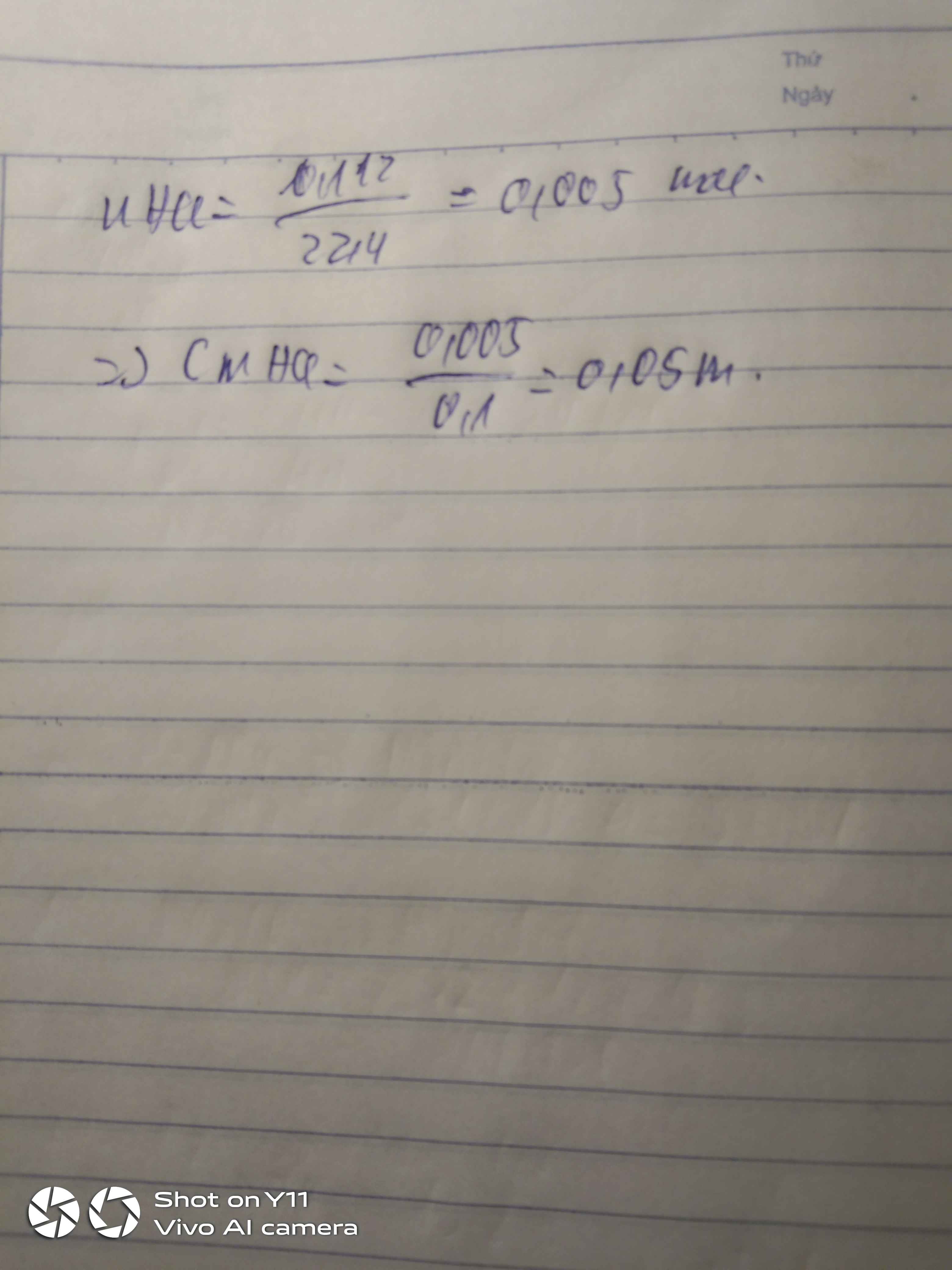

Ta co
mdd=mct + mdm=14,3 + 35,7 = 50 g
Nong do % cua dd la
C% =\(\dfrac{mct}{mdd}.100\%=\dfrac{14,3}{50}.100\%=28,6\%\)
mdd= mdm + mct = 14,3+35,7= 50(g)
C%= mct÷mdd×100% = 14,3÷50×100%=28,6%