Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi CTTQ của muối halogen là MX
PTHH MX + AgNO3 ----> AgX + MNO3
ta có số mol của MX = số mol của AgX
=> \(\dfrac{4,25}{M+X}\)=\(\dfrac{14,35}{108+X}\) <=> 459+4,25X=14,35M+14,35X
<=> 14,35M+10X=459
+ nếu X là Flo thì M=19(kali)
+ nếu X là Clo thì M=7,24 (loại)
tương tự ta bạn tính ra sẽ loại luôn Brom và Iot
vậy muối halogen đó là KF

Đáp án C
Gọi công thức muối cần tìm là MX2.
Khi cho 150 gam dung dịch X tác dụng với dung dịch Na2CO3 dư có phản ứng:
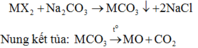
Do đó khí hấp thụ vào dung dịch KOH là CO2.
Vì sau phản ứng trong dung dịch vẫn còn KOH nên sản phẩm tạo thành là K2CO3:
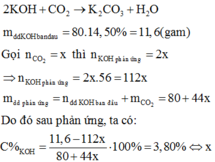 = 0,75
= 0,75

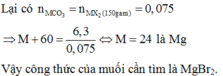

Định làm mà thấy bên dưới có bài y hệt nên thôi nhé
Mà bạn này..Mk thấy mấy bài này kiểu ở lớp 8,9 mà..Sao bạn cứ để ở lớp 10 thế

Chúc bạn học tốt :))

Đáp án C
Hướng dẫn Ta có: ![]()
![]() Cl + AgNO3 →
Cl + AgNO3 → ![]() NO3 + AgCl
NO3 + AgCl
0,13 mol 0,13 mol
=> (![]() + 35,5).0,13 = 6,645 →
+ 35,5).0,13 = 6,645 → ![]() = 15,62
= 15,62
Mà 2 kim loại kiềm thuộc hai chu kì kế tiếp nhau → Li (7) và Na(23)

Cứ 10ml dd X phản ứng với dd AgNO3 dư tạo 0,7175 g kết tủa
\(\Rightarrow\) Với 200ml dd X phản ứng với dd AgNO3 dư tạo \(0,7175\cdot20=14,35\left(g\right)\) kết tủa
PTHH: \(RX+AgNO_3\rightarrow RNO_3+AgX\downarrow\)
Theo phương trình: \(n_{RX}=n_{AgX}\) \(\Rightarrow\dfrac{4,25}{R+X}=\dfrac{14,35}{108+X}\)
Ta thấy với \(\left\{{}\begin{matrix}R=7\\X=35,5\end{matrix}\right.\) thì phương trình trên thỏa mãn
\(\Rightarrow\) Muối cần tìm là LiCl (0,1 mol) \(\Rightarrow C_{M_{LiCl}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)

Bài 3 :
$R_2CO_3 + 2HCl \to 2RCl + CO_2 + H_2O$
n H2O = n CO2 = 6,72/22,4 = 0,3(mol)
n HCl = 2n CO2 = 0,6(mol)
Bảo toàn khối lượng :
m muối = 38,2 + 0,6.36,5 - 0,3.44 + 0,3.18 = 41,5(gam)
Bài 4 :
n H2 = 5,6/22,4 = 0,25(mol)
$Fe + 2HCl \to FeCl_2 + H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
n HCl = 2n H2 = 0,5(mol)
Bảo toàn khối lượng :
m muối = 10 + 0,5.36,5 - 0,25.2 = 27,75(gam)

Gọi M là khối lượng mol trung bình của 2 nguyên tố
nH2=6.72/22.4=0.3 mol
M + H2O --> MOH + 1/2 H2
0.6mol---------------------0.3mol
-> M=20.2/0.3=67.3333
-->M1<67.33<M2
mà 2 kim loại này thuộc hai chu kì liên tiếp nhau
--> Kim loại đó là KI và Rb

Xét 2 trường hợp:
Trường hợp 1: Giả sử hai muối đều tạo kết tủa:
Gọi Z là halogen đại diện
\(NaZ+AgNO3\rightarrow AgZ+NaNO3\)
\(\dfrac{2,9825}{23+Z}\) \(\dfrac{0,7175}{108+Z}\)
\(\Rightarrow\dfrac{2,9825}{23+Z}=\dfrac{0,7175}{108+Z}\Leftrightarrow Z\approx2,4\) ( loại )
Trường hợp 2: Giả sử chỉ có một muối tạo kết tủa:
⇒ Đó là NaF và NaCl
NaF không phản ứng với AgNO3
NaCl + AgNO3 → AgCl + NaNO3
0,005 ← \(\dfrac{0,7175}{108+35,5}\)
mNaCl = 0,005 . ( 23 + 35,5 ) = 0,2925 (g) ( nhận )
Vậy hai nguyên tố X và Y cần tìm là: F và Cl



AB + AgNO3 => AgB + ANO3
A+B ----------------108+B
4.25 ---------------- 14.35
->14.35A+10.1B=459
B la Halogen => B = 35.5(cl) => A = 7(li)
B = 80(Br) => A = -68 (loai)
Vay CT mmuoi A la LiCl
Bn giải tắt quá mik cần thật chi tiết