Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 2H2 + O2 → 2H2O
nH2 = \(\dfrac{11,2}{22,4}\)= 0,5 mol
nO2 =\(\dfrac{6,4}{32}\)= 0,2 mol
Ta có tỉ lệ \(\dfrac{nH_2}{2}\)> \(\dfrac{nO_2}{1}\)=> sau phản ứng hidro dư , oxi hết , tính toán theo oxi.
nH2 phản ứng = 2nO2 = 0,4 mol
=> nH2 dư = nH2 ban đầu - nH2 phản ứng = 0,5 - 0,4 = 0,1 mol
b) nH2O = 2nO2 = 0,4 mol
=> mH2O = 0,4.18 = 7,2 gam
Thầy Bùi Thế Nghị ơi !!
Viết \(\%m_{NT}=\dfrac{m_{NT}}{M_{hc}}.100\%\) thì có 2 khối lượng thì có sai không ạ !! Hay mNT trên tử phải là khối lượng mol ạ thầy

\(n_{H_2}=\dfrac{V_{H_2}}{22,4}=\dfrac{11,2}{22,4}=0,5mol\)
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{8}{22,4}=0,35mol\)
\(2H_2+O_2\rightarrow\left(lửa.điện\right)2H_2O\)
0,5 > 0,35 ( mol )
0,5 0,25 0,5 ( mol )
\(m_{H_2O}=n_{H_2O}.M_{H_2O}=0,5.18=9g\)
\(V_{H_2O}=9l\)
\(m_{O_2\left(dư\right)}=n_{O_2\left(dư\right)}.M_{O_2}=\left(0,35-0,25\right).32=3,2g\)

\(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2mol\)
4P + 5O2 \(\underrightarrow{t^o}\) 2P2O5
\(\dfrac{0,1}{4}< \dfrac{0,2}{5}\) => O2 dư, Photpho đủ
\(n_{O_2}=0,2-0,04=0,16\left(mol\right)\)
\(m_{P_2O_5}=\) 0,05 . 142 = 7,1 ( g )

Gọi x, y lần lượt là số mol của Cu và Fe.
Ta có: \(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a. PTHH: 2Cu + O2 ---to---> 2CuO (1)
3Fe + 2O2 ---to---> Fe3O4 (2)
Ta có: \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
Theo PT(1): \(n_{Cu}=n_{CuO}=0,2\left(mol\right)\)
Theo PT(1): \(n_{O_2}=\dfrac{1}{2}.n_{Cu}=\dfrac{1}{2}x\left(mol\right)\)
Theo PT(2): \(n_{O_2}=\dfrac{2}{3}.n_{Fe}=\dfrac{2}{3}y\left(mol\right)\)
=> \(\dfrac{1}{2}x+\dfrac{2}{3}y=0,3\)
Mà nCu = 0,2(mol)
Thay vào, ta được: \(\dfrac{1}{2}.0,2+\dfrac{2}{3}y=0,3\)
=> y = 0,3(mol)
=> \(m_{Cu}=0,2.64=12,8\left(g\right)\)
\(m_{Fe}=0,3.56=16,8\left(g\right)\)
b. \(\%_{Cu}=\dfrac{12,8}{12,8+16,8}.100\%=43,24\%\)
\(\%_{Fe}=100\%-43,24\%=56,76\%\)

a)
nO2=8.96/22,4=0.4 mol
---->mO2=0.4*32=12.8g
nCO2=4.48/22.4=0.2 mol
---->mCO2=0.2*44=8.8g
Áp dụng định luật bảo toàn khối lượng:
mA+mO2=mCO2+mH2O
---->mA=mCO2+mH2O-mO2=8.8+7.2-12.8=3.2g
b) Gọi CTPT của A là CxHy
4CxHy + (4x+y)O2-----> 4xCO2 + 2yH2O
Ta có:
dMA/MHe=(12x+y)/4=4
---->MA=12x+y=16(1)
nCxHy=1/x*nCO2=0.2/x=3.2/16=0.2mol(2)
-----> x=1 ; y=4
Vậy CTPT của A là CH4

a, Theo gt ta có: $n_{H_2}=0,15(mol);n_{O_2}=0,05(mol)$
$2H_2+O_2\rightarrow 2H_2O$
Sau phản ứng $H_2$ còn dư. Và dư 0,05.22,4=1,12(l)
b, Ta có: $n_{H_2O}=2.n_{O_2}=0,1(mol)\Rightarrow m_{H_2O}=1,8(g)$

$a) CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
b) $n_{CH_4} = \dfrac{3,92}{22,4} = 0,175(mol)$
$n_{O_2} = \dfrac{3,84}{32} = 0,12(mol)$
Ta thấy : $n_{CH_4} : 1 > n_{O_2} : 2$ nên $CH_4$ dư
$n_{CH_4\ pư} = \dfrac{1}{2}n_{O_2} = 0,06(mol)$
$\Rightarrow m_{CH_4\ dư} = (0,175 - 0,06).16 = 1,84(gam)$
c) $2NaOH + CO_2 \to Na_2CO_3 + H_2O$
Theo PTHH :
$n_{Na_2CO_3} = n_{CO_2} = \dfrac{1}{2}n_{CH_4} = 0,06(mol)$
$m_{Na_2CO_3} = 0,06.106 = 6,36(gam)$

a)
\(V_{H_2} = V_{O_2} = \dfrac{4,48}{2} = 2,24(lít)\)
b)
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ V_{H_2} = 2,24 < 2V_{O_2} = 4,48(lít)\)
Do đó, O2 dư.
\(V_{O_2\ pư} = \dfrac{1}{2}V_{H_2} = 1,12(lít)\\ \Rightarrow V_A = V_{O_2\ dư} = 2,24 - 1,12 = 1,12(lít)\)
a, Theo bài ra ta có : \(\left\{{}\begin{matrix}V_{H2}+V_{O2}=4,48\\V_{H2}=V_{O2}\end{matrix}\right.\)
\(\Rightarrow V_{O2}=V_{H2}=2,24\left(l\right)\)
b, Ta có : \(n_{O_2}=n_{H_2}=\dfrac{V}{22,4}=0,1\left(mol\right)\)
\(PTHH:2H_2+O_2\rightarrow2H_2O\)
Thấy sau phản ứng O2 dư .
=> \(V_A=V_{O2du}=22,4\left(n_{o2}-n_{O2pu}\right)=1,12\left(l\right)\)
Vậy ..
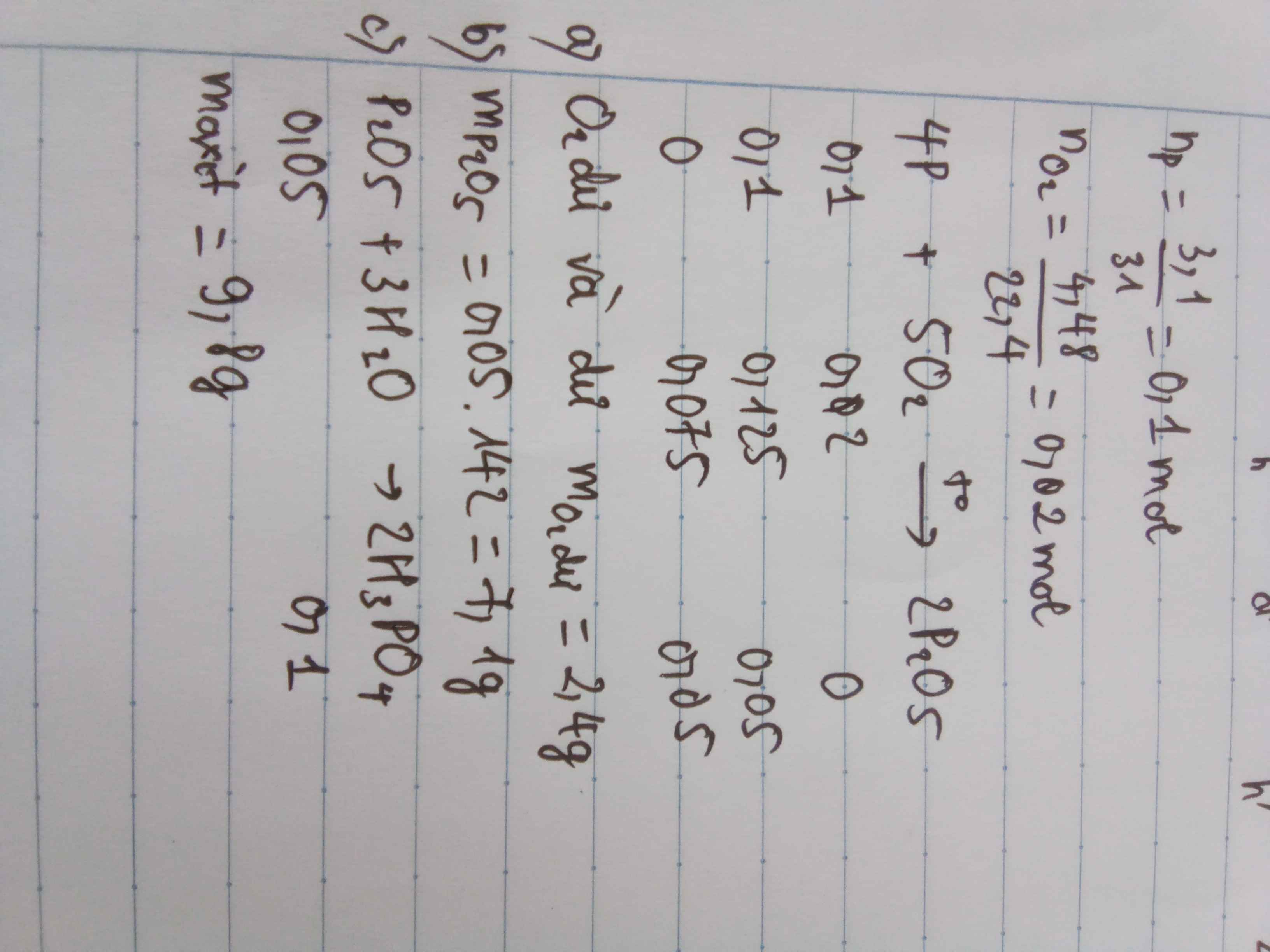
a)PTHH: 2H2 + O2 -> 2H2O
Theo đề , ta có: VH2 + VO2 =4,48
=> VH2 =VO2 =\(\dfrac{4,48}{2}=2,24\left(l\right)\)
=> nH2 = nO2 =\(\dfrac{2,24}{22,4}0,1\left(mol\right)\)
Ta có tỉ lệ: \(\dfrac{n_{H2}}{2}=\dfrac{0,1}{2}=0,05< \dfrac{n_{O2}}{1}=0,1\)
=> H2 hết, O2 dư
Vậy tính số mol các chất cần tìm theo H2
Theo PT: nO2 =\(\dfrac{1}{2}nH2=\dfrac{1}{2}.0,1=0,05\left(mol\right)\)
=>nO2dư = 0,1-0,05=0,05(mol)
=>mO2dư = 0,05.32=1,6(g)
b) Theo PT: nH2O = nH2 = 0,1(mol)
=>mH2O = 0,1.18 = 1,8(g)