Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

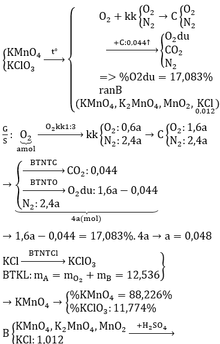
PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\) (1)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\) (2)
\(C+O_2\underrightarrow{t^o}CO_2\) (3)
Ta có: \(n_{KCl}=\dfrac{1,49}{74,5}=0,02\left(mol\right)\)
\(n_C=\dfrac{0,24}{12}=0,02\left(mol\right)\)
\(m_Y=\dfrac{1,49}{17,028\%}=8,75\left(g\right)\), Y gồm: KCl, KMnO4 (dư), K2MnO4, MnO2.
Theo PT (3): \(n_{CO_2}=n_{O_2\left(pư\right)}=n_C=0,02\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{0,02}{40\%}-0,02=0,03\left(mol\right)\)
⇒ ΣnO2 = 0,02 + 0,03 = 0,05 (mol)
Theo PT (1): \(n_{O_2\left(1\right)}=\dfrac{3}{2}n_{KCl}=0,03\left(mol\right)\)
\(\Rightarrow n_{O_2\left(2\right)}=0,05-n_{O_2\left(1\right)}=0,02\left(mol\right)\)
Theo PT (2): \(n_{K_2MnO_4}=n_{MnO_2}=n_{O_2\left(2\right)}=0,02\left(mol\right)\)
\(n_{KMnO_4\left(pư\right)}=2n_{O_2}=0,04\left(mol\right)\)
Mà: mKCl + mKMnO4 (dư) + mK2MnO4 + mMnO2 = 8,75
⇒ mKMnO4 (dư) = 1,58 (g) \(\Rightarrow n_{KMnO_4\left(dư\right)}=\dfrac{1,58}{158}=0,01\left(mol\right)\)
\(\Rightarrow H\%=\dfrac{0,04}{0,04+0,01}.100\%=80\%\)

\(n_{C_2H_4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\\ n_{O_2}=3.0,4=1,2\left(mol\right);n_{CO_2}=0,4.2=0,8\left(mol\right)\\ a,V_{O_2\left(đktc\right)}=22,4.1,2=26,88\left(l\right)\\ b,V_{kk\left(đktc\right)}=\dfrac{100}{20}.26,88=134,4\left(l\right)\\ c,CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow\left(trắng\right)+H_2O\\ n_{CaCO_3}=n_{CO_2}=0,8\left(mol\right)\\ m_{kết.tủa}=m_{CaCO_3}=100.0,8=80\left(g\right)\)

A tác dụng với NaHCO3 cho khí CO2 → A: axit CH3COOH
BTKL: m + mO2 = mCO2 + mH2O => m = 1,8
=> nCH3COOH = 0,03
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
0,03 0,02 0,0125
=> H = 62,5%

Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)

Bài 2:
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
PTHH: 4P + 5O2 → 2P2O5
Mol: 0,4 0,2
\(m_{P_2O_5}=0,2.142=28,4\left(g\right)\)
Bài 1:
\(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
PTHH: 4Al + 3O2 ---to→ 2Al2O3
Mol: 0,4 0,3
\(V_{O_2}=0,3.22,4=6,72\left(l\right)\)
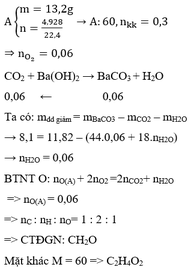
a) $n_{Cu} = \dfrac{12,8}{64} = 0,2(mol)$
$n_{O_2} = \dfrac{33,6.20\%}{22,4} = 0,3(mol)$
$2Cu + O_2 \xrightarrow{t^o} 2CuO$
$n_{Cu} : 2 < n_{O_2} :2$ nên Oxi dư
$n_{CuO} = n_{Cu} = 0,2(mol)$
$m_{CuO} = 0,2.80 = 16(gam)$
b)
$n_{O_2\ pư} = \dfrac{1}{2}n_{Cu} = 0,1(mol)$
$m_{O_2\ dư} = (0,3 - 0,1).32 = 6,4(gam)$